吴祖泽:干细胞临床应用 政策还差临门一脚

2014中国生物治疗大会现场,细胞治疗应用审批问题最受参会人员关注。在回答有关代表提问时,吴祖泽院士曾表示,专家委员会已呈递相关意见,希望大家一起呼吁政府部门加快转化医学步伐。
2015年8月,《干细胞临床研究管理办法(试行)》发布。这一文件的出台有何现实意义?干细胞治疗有着怎样的前景?近日,在2015中国生物治疗大会召开前夕,吴祖泽院士就以上问题接受了《医师报》记者专访。
干细胞临床研究有了“底线”
《医师报》:今年8月,《干细胞临床研究管理办法(试行)》发布。这一文件的亮点在哪里?
吴祖泽:文件特别强调干细胞治疗必须具备的三个基本条件,并且提到自体干细胞与异体干细胞治疗都应符合本办法。
2011年前后,我国干细胞研究和治疗在国内外产生了比较好的影响,同时也存在管理混乱的局面。为规范这一现状,2011年12月,原卫生部下发《关于开展干细胞临床研究和应用自查自纠工作的通知》,明确要求各省停止未经原卫生部和原国家食品药品监督管理局批准的干细胞临床研究和应用活动,且暂不受理任何申报项目。
当时我们采取“一刀切”的办法,在规范整顿的同时,也不可避免地影响了干细胞临床研究和产业化发展。“一刀切”文件下发后,为探索建立监管模式和长效机制, 2012年5月,国家又组织成立了专家委员会。三年多的时间里,专家委员会召开十次会议,《干细胞临床研究管理办法(试行)》(以下简称《管理办法》)终于在2015年8月正式出台。
《管理办法》为三级医疗机构选择开展干细胞临床研究项目提供了依据。即,开展干细胞临床研究必须具备三个基本条件:安全、有效,更关键的一点是开展的技术,其预防或治疗疾病的效果要优于现有手段,或现有医疗技术尚不能解决的适应证。
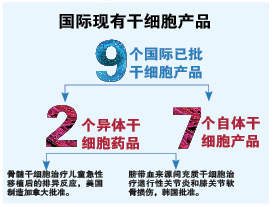
用于治疗的干细胞根据排异性的不同,可分为两类,一类是自体干细胞,来源于受体自身,另一类是异体干细胞,来源于他人。自体干细胞数量少,一般仅供个人使用,异体干细胞数量丰富,可供人群使用,最终可转化为临床大规模应用。国际上已有异体干细胞药品。
《管理办法》的出台,体现了细胞治疗发展要兼顾自体干细胞和异体干细胞的思路,文件对两类细胞的能力标准与安全标准是一样的。
政策空白致使产业停顿
《医师报》:干细胞临床研究方面,国家政策已有进步。在产业化方面,是否也有突破呢?
吴祖泽:除造血干细胞以外,我国干细胞技术临床应用审批监管政策仍是空白。
我国干细胞药物0上市
然而,我国产业化步伐显得有些落后。2004年12月,原国家食品药品监督管理局下发第一个干细胞药物临床试验批件。至今10余年间,没有一个获准上市。最新的《管理办法》仍没能给出研究后的出口。
办法后的“试行”二字说明临床研究后还有很多问题,例如业内最关心的临床研究如何转化为应用的问题,具体途径仍然没有明确。
理解这个《管理办法》,不能仅停留在研究阶段,应通过这个管理办法,进一步发展干细胞临床应用和干细胞产业,解决临床问题。并且,解决问题的途径不仅仅是个体化,更希望能成为药品。在研究出口方面,大家意见并没有统一。 药品需要很强的政策性,不能没有指导地往下走,但也不能静止等待。
政策空白是产业停顿原因
至今国内仍没有批准应用的干细胞产品,而这并不是因为技术能力达不到水准,而是缺少这方面的政策。业内人士不明白干细胞产品、药品应该由哪一个部门进行备案,到底是谁来接受申请和咨询。
现实中,不少医院都在开展骨髓移植,不可避免会产生排斥反应,干细胞治疗是很重要的办法。此项技术临床上应用已经表明是安全有效的,有些医院甚至已经向国家有关部门申报了干细胞治疗技术或药品,但是由于缺少管理的办法,一直处于停顿状态。
对于这些成熟的干细胞技术,临床研究和临床应用早就应该开放,但从“一刀切”至今的4年多时间里,我们一直处于不清醒的状态,耽误了患者的治疗,同时也耽误了我们国家产业的发展壮大。
国家应该加快对临床上已成熟的干细胞技术的审批。国家卫生计生委和食品药品监督管理总局已经做了相关准备工作,问题是我们现在需要加快步子,设立一个组织专门来管理这类科技产品。
探索应用规范 细胞质量先行
《医师报》:细胞治疗规范方面,还有哪些问题亟需解决?
吴祖泽:应当探索加强细胞质量和监管的途径。
在很长一段时间内,国内有大大小小的企业和医院都来生产临床用细胞,一方面增加了卫生行政部门对生产过程的监管难度,另一方面生产的细胞质量得不到保障,隐藏着生命健康威胁。细胞治疗如何规范一直是行业内关心的问题。
我作为中国医药生物技术协会再生医学专业分会主任委员,在2011年我为此提出了5点意见,包括加强领导监管、制定管理规范标准等,其中第4点意见为加强细胞质量和监管提出了具体探索路径。即,对于已经成熟的项目,不管是干细胞还是免疫细胞可考虑择优建立区域性细胞生产供应基地,用于临床应用和研究。生产基地可以设在具有研究性的三甲医院,也可以设在企业,但是相应机构必须合乎细胞生产车间标准,生产细胞必须符合细胞质量标准。
这些年,我在学术交流中不断呼吁区域性细胞生产供应基地。这一建议也正在慢慢被接受,如今在深圳、南昌市等地,已有当地卫计委、发改委、食品药品管理部门联合签发的文件支持区域性细胞发展。
“后起之秀”CART免疫细胞
《医师报》:细胞治疗容易在哪些疾病方面取得突破?
吴祖泽:目前,临床上有运用造血干细胞技术治疗白血病和再生障碍性贫血。大量的调研结果看出免疫细胞治疗肿瘤有良好的辅助效果。
细胞治疗分为干细胞治疗和体细胞治疗。干细胞又分为成体干细胞和胚胎干细胞。目前,临床上应用的主要是骨髓来源的成体干细胞。
骨髓造血干细胞技术是国家二类医疗技术,临床上常用于治疗白血病和再生障碍性贫血。间充质干细胞技术适应证较广,究竟哪一个适应证可以发展成为干细胞产品,需要进行安全有效性研究。目前我国还没有一个间充质干细胞技术治疗疾病,优于现有技术。不过,现在国外在进行大量的研究,有上百个适应证等着审批,中国还没批准一个。
此外,体细胞的应用主要是免疫细胞。现在出现的CART细胞是一类靶向性免疫细胞,其对B淋巴细胞白血病的治疗超出了以往水平,能否扩展到实体瘤受到大家关注。

发表评论
最新评论


