连花清瘟胶囊治疗新型冠状病毒肺炎无症状感染者的有效性:一项随机、对照多中心试验
张玲1,#,武蕾2,#,徐霄龙3,#,袁雅冬4,蒋荣猛5,阎锡新4,张鑫1,高勇1,商焕霞1,胡晶3,王雪瑞3,梅建强2,*,吴树才1,*,刘清泉3,*
1. 河北省胸科医院,石家庄050041;
2. 河北省中医院,石家庄050011;
3. 首都医科大学附属北京中医院,北京100010;
4. 河北医科大学第二医院,石家庄050000;
5. 首都医科大学附属北京地坛医院,北京100015;
关键词: COVID-19,无症状患者,连花清瘟,疗效,临床试验
摘要
背景:新型冠状病毒病(COVID-19) 无症状感染者由于病毒载量高,是传播链中不可忽视的来源。然而,基于有症状的治疗方案似乎不适用于无症状感染患者。在这项研究中,作者希望评估连花清瘟胶囊对无症状COVID-19感染患者的疗效。
方法:采取随机对照试验(RCT)的方法,探讨连花清瘟胶囊治疗无症状 COVID-19 患者的有效性和安全性。患者被随机分为对照组(隔离观察组)和治疗组(连花清瘟,4 粒,每日三次),疗程14 天。主要研究终点是隔离观察期间的核酸转阴时间和转阴率。
结果:120名受试者被纳入全分析集(对照组和治疗组各60名)。数据显示,治疗组隔离观察期间核酸转阴率高于对照组(率差:21.66%,95%[CI]:4.34~37.27,p =0.0142)。治疗组患者核酸转阴时间相对对照组较短(7.5 天 vs. 14.5 天, p = 0.018)。此外,治疗组临床症状出现率低于对照组(率差异:-31.67,95% CI:-46.83 ~-13.82, p = 0.0005)。治疗组转为确诊轻症和普通病例的比例也较低(35.00% vs. 66.67%,p= 0.0005)。并无记录严重不良事件。
结论:在本研究中,作者阐明了连花清瘟胶囊对无症状新型冠状病毒(COVID-19)感染患者的有益作用。考虑到现阶段缺乏治疗无症状 COVID-19 患者的干预措施,连花清瘟胶囊可以考虑作为一种新的选择。
中国临床试验注册中心:ChiCTR2100042066。
背景介绍
自 2019 年以来,新型冠状病毒肺炎(COVID-19)大流行已在全球蔓延,主要通过人际传播,并导致重大公共卫生问题。1迄今为止,世界卫生组织 (WHO) 的公开数据显示,严重急性呼吸系统综合症冠状病毒 2 (SARS-CoV-2) 已感染超过2亿人,并确认 400 万人死亡。由于COVID-19 的治疗药物有限,干预措施必须更多地依赖于追踪密接者、隔离和保持社交距离。考虑到 SARS-CoV-2 的快速传播和不可预测的变异性,未来5年COVID-19疾病的总发病率将保持在较高水平,并有机会成为常态化2。这对我们的医疗系统,尤其是重症监护病房 (ICU)的容量无疑是一个巨大的挑战。因此,寻找更多的互补性干预措施以减少ICU需求是非常重要的。3
最初,COVID-19患者一般分为轻症、普通、重症和危重症4类,这4类患者是最受关注且医疗资源最多的4。然而,越来越多的病例报告记录了PCR检测呈阳性但没有典型临床症状或体征的患者1,5。随着对SARS-CoV-2病毒发病机制和流行病学的深入了解,COVID-19无症状患者被认为是一个庞大的群体。更重要的是,这些无症状患者具有同样高的传染性和隐蔽性6。因此,无症状感染是不可忽视的感染传播链。
目前,针对COVID-19的药物研发遇到了瓶颈。据报道,许多有希望的抗病毒疗法对 COVID-19 住院患者的效果有限。7对于无症状感染者,由于没有典型症状,干预难度更大。目前,对潜伏期COVID-19患者的建议医学观察期最长为14天。8如果没有有效的治疗,这些患者很有可能发展成临床确诊病例。中医药 (TCM) 作为补充和替代医学在中国 COVID-19 流行中发挥了重要作用。9-11连花清瘟胶囊是中国国家卫健委正式推荐的治疗COVID-19具有专利的中成药。它已证实对症状轻微、常见和严重的 COVID-19 感染患者有效。12-15然而,它是否对无症状患者有显著的有益作用,还需要验证。
在这项试验中,作者进行了一项随机、对照的多中心试验,旨在探索 连花清瘟 胶囊治疗无症状新型冠状病毒感染患者的有效性和安全性。考虑到无症状患者急需有效的治疗方法,本研究可能为连花清瘟胶囊作为临床潜在选择提供更多的证据支持。
研究方法
研究设计
这是一项随机、对照、多中心的新冠肺炎无症状感染者的临床试验。本研究共纳入120例患者,随机分为治疗组和对照组。该研究已获河北省胸科医院伦理委员会批准(No.2021003)。严格遵守GCP准则和赫尔辛基宣言。该研究已在中国临床试验注册中心(ChiCTR2100042066)注册。已取得患者或法定代表人的书面知情同意。随机对照试验应报告的对照检查清单的信息已在补充表格S1中列出。
患者
纳入标准如下:
1) 病原学检测确诊为无症状新型冠状病毒肺炎感染患者;
2) 年满18周岁(含18周岁);
3) 在研究开始前自愿签署知情同意书。
排除标准为:
1) 病原学检测并有临床表现或体征确诊的新型冠状病毒肺炎患者;
2) 在研究者看来,患有恶性疾病、自身免疫性疾病、肝肾疾病、血液疾病、神经系统疾病、内分泌疾病等严重疾病的患者可能会影响患者参与试验或影响研究结果;
3) 孕妇、哺乳期妇女;
4) 最近3个月内参加过其他临床试验的患者;
5) 有过敏症状,如对两种或两种以上药物或食物过敏史,或已知对药物成分过敏;
6) 研究者认为存在不适合入组或影响疗效评价的因素。
2021年1月1日至3月31日,共有3家医院(河北省胸科医院、邢台市第二医院、哈尔滨市传染病医院)的120名患者参与了本试验。所有患者均未接种疫苗。分别于第0天、第7天和第14天进行随访。
临床分型
所有患者在试验开始时均无症状。在试验结束时,患者被分为四种类型,包括无症状病例、轻度病例、普通病例和重症病例。无症状:没有临床症状的确诊病例;轻度:确诊病例有发热(测量或主观)或呼吸道症状;普通:有发热(测量或主观)或呼吸道症状的确诊病例,以及肺炎的放射学证据;重症:确诊病例有发热、呼吸道症状、肺炎影像学证据,并至少有以下症状之一:(1)呼吸窘迫,呼吸频率≥30次/min;(2) 静息状态,平均氧饱和度≤93%;(3) PaO2/FiO2≤300 mmHg(1 mmHg = 0.133 kPa)。
样本量计算
本研究的主要目的是研究有或无连花清瘟胶囊治疗的无症状 COVID-19患者的 核酸转阴率。作者根据我国临床经验假设治疗组转阴性率为50%,对照组为25%。治疗组和对照组患者按1:1的比例分配(a = 0.05 [双方] 把握度 = 0.80)),根据功率分析和样本量15.0计算,总样本量为110例。假设退出率<10%,本研究的总样本量最终设定为120个,其中治疗组60例,对照组60例。
随机化和分组
本试验采用区组随机化方法,随机化数字通过 SAS 9.4 软件( 9C1XJD;SAS Institute)生成。共120例患者分为治疗组和对照组。采用基于计算机的 1:1 区组随机化方法将病例分别分配到治疗组和对照组。随机化的分组长度为4。随机化列表由统计学家保存。为确保分配隐藏,随机化的细节通过使用顺序编号的不透明密封信封分发给临床医生。
每个连续编码的患者由临床医生随机招募和编号,直到达到预设的病例数。所有主治临床医师均取得国家药品监督管理局临床试验资格。第三方数据分析由华中科技大学专业统计学家独立完成。统计学家和结果评估员均不知分组情况。
研究药物
对照组按照国家卫健委发布的《新型冠状病毒感染的肺炎诊疗方案(试行第八版)》进行隔离。16根据《中华人民共和国药典》,连花清瘟胶囊的主要成分如下:金银花、连翘、大黄、板蓝根、炙麻黄、广藿香、薄荷脑、甘草、红景天、绵马贯众、鱼腥草和石膏。治疗组患者隔离后口服连花清瘟胶囊(批号B2012037,每粒0.35g,4粒,每日三次),连服14天。一旦发展为临床确诊病例,受试者将转入医院常规治疗,并记录在试验数据中。
研究终点
主要终点为隔离观察期间根据PCR检测(批号:20040999;大安基因,中国广州)核酸转阴的时间和比率。次要终点包括临床症状及严重程度、临床症状出现时间和比例、隔离观察期间确诊的新型冠状病毒肺炎轻症和普通病例比例、血常规、生化指标等。(根据COVID-19 患者的诊断和治疗方案(试验第八版)(补充文件S2)
安全性
记录了试验期间发生的不良事件 (AE),无论是否与研究药物有因果关系。
统计分析
所有统计分析均使用 SAS 9.4 软件(订单号 9C1XJD;SAS Institute)进行。通过使用包括所有随机分配的患者的完整分析集(FAS)测量和评估主要结果。还进行了仅限于遵循方案并完成试验的患者的符合方案集 (PPS) 分析。对于描述性分析,计数数据由病例数和构成比描述。测量数据用平均值、标准偏差、最大值和最小值来描述。非正态分布的数据由中位数和第 25 和第 75 个分位数描述。
有效性分析,对主要疗效指标“核酸转阴率”试验组与对照组的比较进行优效检验,并采用Newcombe-Wilson法计算率差的95%CI,如果95%CI的下限大于0,则可认为有效性成立。核酸转阴时间采用Log-Rank检验比较组间差异。
安全性分析(SS集)用于进行安全性评估。对本研究中发生的 AE 进行了描述性统计。列出了每组中发生 AE 和不良反应的患者人数及其百分比。使用χ 2检验或Fisher精确概率法比较组间AE的发生率。
结果
患者特征
试验的流程图如图 1 所示。2021 年 1 月 1 日至 3 月 31 日,该试验共纳入 120 例无症状 COVID-19 病例并随机分组,对照组和治疗组各 60 例。没有受试者提前永久退出试验。两组在发病时的年龄、性别、体格、体温和流行病学统计方面具有可比性(表 1)。
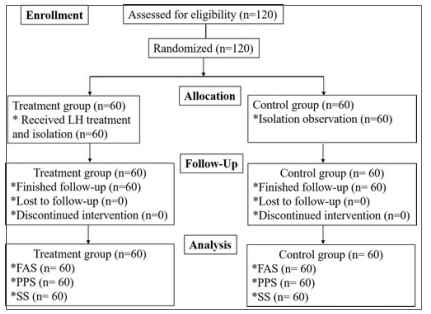
表 1.基线人口统计数据
项目 | 治疗组(N = 60) | 对照组(N = 60) |
年龄(yr, x ± s) | 41.07 ±13.49 | 44.85 ± 15.41 |
性别(N, %) 身高 (cm, x ± s) 体重 (kg, x ± s) 体温(℃, x ± s) 呼吸 (bpm, x ± s) | 31(51.67) 167.40±8.86 66.26±13.88 36.47 ± 0.37 18.40 ± 2.07 | 31(51.67) 166.90±7.69 63.76±10.46 36.51±0.36 18.87 ± 2.02 |
脉搏 (times/min, x ± s) 收缩压 (mmHg, x ± s) 舒张压 (mmHg, x ± s) 14天内接触过确诊患者(N, %) 聚集性发病 (N, %) | 79.35 ±10.12 131.58±19.43 85.65±13.85 26(43.33) 38(63.33) | 82.35 ±9.27 136.23±18.74 85.98±13.42 27(45.00) 41(68.33) |
主要终点
治疗组14天核酸转阴率高于对照组(FAS:48.33% vs. 26.67%,率差:21.66%,95% CI:4.34~37.27,p=0.0142;PPS与 FAS 相同)(表 2)。同时,治疗组核酸转阴时间较对照组短(FAS:7.5 vs. 14.5天,p =0.018)(图2)。
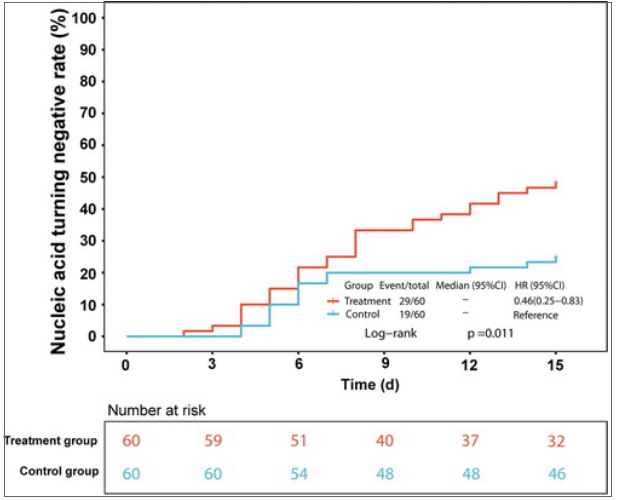
如图。2. FAS中核酸转阴率的动态变化。红线和蓝线分别代表治疗组和对照组。CI,置信区间;FAS,全分析集。
表 2.核酸转阴率(FAS)
结局指标 | 治疗组(N = 60) | 对照组(N = 60) |
阴性,n (%) | 29 (48.33) | 16 (26.67) |
阳性,n (%) | 31 (51.67) | 44 (73.33) |
p | 0.0142 | |
率差(治疗-对照)和 95% CI | 21.66(4.34 至 37.27) | |
注: 95% CI 的比率差异是通过 Newcombe-Wilson 方法计算的。p<0.05表示两组之间存在显著差异。CI,置信区间。
次要终点
与对照组相比,治疗组在隔离观察期间出现临床症状的比例较小(FAS:35.00% vs. 66.67%,率差:-31.67,95% CI:-46.83至-13.82,p = 0.0005)。此外,治疗组出现临床症状的时间更长(图 3;FAS:6.0 天对 2.0 天,p < 0.0001)。与对照组相比,治疗组少数患者发展为轻度(FAS:6.67% vs. 8.33%)或普通型(FAS:28.33% vs. 58.34%)(表3)。
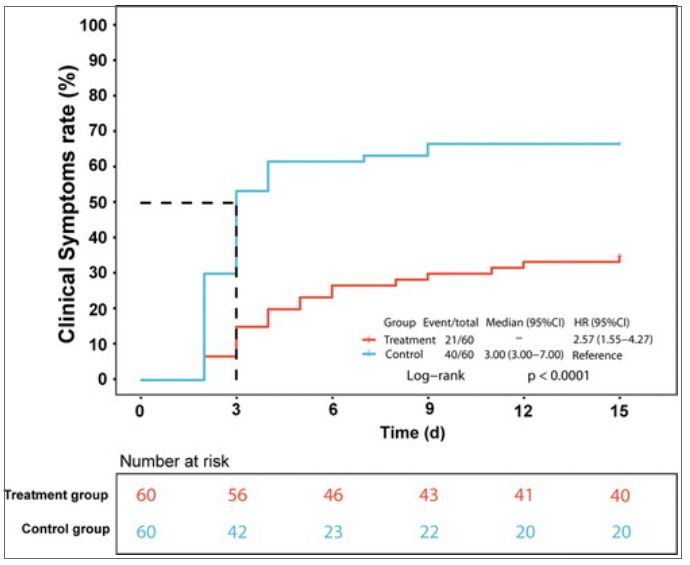
如图。3. FAS中临床症状率的动态变化。红线和蓝线分别代表治疗组和对照组。CI,置信区间;FAS,全分析集;HR,风险比。
表 3.临床症状发生率和分类(FAS)
结局指标 | 治疗组(N = 60) | 对照组(N = 60) |
有症状,n (%) | 21 (35.00) | 40 (66.67) |
无症状,n (%) | 39 (65.00) | 20 (33.33) |
p | 0.0005 | |
率差(治疗-对照)和 95% CI | -31.67(-46.83 至 -13.82) | |
轻度或普通型 | 21 (35.00) | 40 (66.67) |
未分型 | 39 (65.00) | 20 (33.33) |
p值 | 0.0005 | |
率差(治疗-对照)和 95% CI | -31.67(-46.83 至 -13.82) | |
注: 95% CI 的比率差异是通过 Newcombe-Wilson 方法计算的。p<0.05表示两组之间存在显着差异。CI,置信区间。
与对照组相比,治疗组隔离观察发热发生率较低(FAS:6.67% vs. 30.00%,p=0.0010)。治疗组的乏力发生率也有所降低(FAS:6.67% vs. 20.00%,p= 0.0317)。通过分析呼吸道症状的发生率, 观察到治疗组咳嗽(FAS:23.33% vs. 46.67%,p = 0.0074)和咳痰(FAS:8.33% vs. 23.33%,p= 0.0074)的发生率与对照组比较较低(表 4)。
表 4.临床症状发生情况(FAS)
指标 | 发生率 | 治疗组 ( N = 60), n (%) | 对照组 ( N = 60), n (%) |
发烧 | 发生 | 4 (6.67) | 18 (30.00) |
没有发生 | 56 (93.33) | 42 (70.00) | |
p值 | 0.0010 | ||
乏力 | 发生 | 4 (6.67) | 12 (20.00) |
没有发生 | 56 (93.33) | 48 (80.00) | |
p值 | 0.0317 | ||
咳嗽 | 发生 | 14 (23.33) | 28 (46.67) |
没有发生 | 46 (76.67) | 32 (53.33) | |
p值 | 0.0074 | ||
咳痰 | 发生 | 5 (8.33) | 14 (23.33) |
没有发生 | 55 (91.67) | 46 (76.67) | |
p值 | 0.0244 | ||
气促 | 发生 | 3 (5.00) | 6 (10.00) |
没有发生 | 57 (95.00) | 54 (90.00) | |
p值 | 0.2985 | ||
胸闷 | 发生 | 5 (8.33) | 11 (18.33) |
没有发生 | 55 (91.67) | 49 (81.67) | |
p值 | 0.1071 | ||
呼吸困难 | 发生 | 0 (0.00) | 0 (0.00) |
没有发生 | 60 (100.00) | 60 (100.00) | |
p值 | — | ||
头痛 | 发生 | 2 (3.33) | 3 (5.00) |
没有发生 | 58 (96.67) | 57 (95.00) | |
p值 | >0.99 | ||
恶心 | 发生 | 0 (0.00) | 0 (0.00) |
没有发生 | 60 (100.00) | 60 (100.00) | |
p值 | — | ||
呕吐 | 发生 | 0 (0.00) | 0 (0.00) |
没有发生 | 60 (100.00) | 60 (100.00) | |
p值 | — | ||
腹泻 | 发生 | 1 (1.67) | 0 (0.00) |
没有发生 | 59 (98.33) | 60 (100.00) | |
p值 | >0.99 | ||
食欲减退 | 发生 | 0 (0.00) | 0 (0.00) |
没有发生 | 60 (100.00) | 60 (100.00) | |
p值 | — | ||
干啰音 | 发生 | 0 (0.00) | 0 (0.00) |
没有发生 | 60 (100.00) | 60 (100.00) | |
p值 | — | ||
湿啰音 | 发生 | 0 (0.00) | 0 (0.00) |
没有发生 | 60 (100.00) | 60 (100.00) | |
p值 | — | ||
注:p值:治疗组与对照组比较,p值<0.05表示差异显着。
安全性
安全性研究结果总结在表 5中。两组AEs发生率相似,治疗组和对照组分别为1.67%和3.33%(p >0.99)。在治疗组中,据报道一名患者有轻度胃肠功能障碍,并已确认与 连花清瘟 治疗有关。在对照组中,两名患者分别患有轻度眼病和中度胃肠功能障碍,与治疗无关。两组均未报告死亡病例。
表 5.不良事件
不良事件 | 治疗组 ( N = 60), n (%) | 对照组 ( N = 60), n (%) | p值 |
整体 | 1 (1.67) | 2 (3.33) | >0.99 |
眼病 | 0 (0.00) | 1 (1.67) | |
胃肠功能障碍 | 1 (1.67) | 1 (1.67) | |
严重性 | 0.6667 | ||
轻度 | 1 (1.67) | 1 (1.67) | |
中度 | 0 (0.00) | 1 (1.67) | 0.3333 |
重度 | 0 (0.00) | 0 (0.00) | |
与试验药物关系 | 1.0000 | ||
肯定有关系 | 1 (1.67) | 0 (0.00) | |
可能相关 | 0 (0.00) | 0 (0.00) | |
绝对不相关 | 0 (0.00) | 2 (3.33) | |
应该没有关系 | 0 (0.00) | 0 (0.00) | |
不确定 | 0 (0.00) | 0 (0.00) | |
死亡 | 0 (0.00) | 0 (0.00) |
注:p值:治疗组与对照组比较,p<0.05表示差异显着。
讨论
2019年以来,新冠肺炎疫情的爆发和大流行,给全球社会带来了巨大变化和影响。医疗资源多用于新型冠状病毒感染的预防和治疗。与此同时,社交也发生了变化,以远程的形式进行。根据哈佛大学研究人员进行的传播动力学研究,我们必须与SARS-CoV-2病毒共存至少5年2。然而,目前仍然没有有效的干预措施或药物来阻止这一流行病。一项由世卫组织发起涉及11330名COVID-19患者的试验表明,四种最有希望的抗病毒药物,包括瑞德西韦、羟氯喹、洛匹那韦和干扰素治疗,对COVID-19住院患者几乎没有或没有影响7。此外,一项来自中国的临床试验报告称,COVID-19疫苗可以诱导体内产生抗体,但在无症状和有症状感染者中,约90%的人IgG以及中和抗体水平会下降17。
越来越多的证据表明,无症状感染者在COVID-19感染中占的比例很大。根据不同国家最新报告,约30~50%的患者为无症状感染者18 ~ 20。更严重的是,无症状患者和有症状患者的病毒载量相似,提示其具有潜在的不可忽视的传播传染性21。但这些无症状感染者在防疫工作中容易被忽视,因为缺乏支持对症治疗的临床证据,针对住院确诊患者制定的治疗措施和方法不适用于无症状感染者。
由于无症状感染药物研发的重要性和紧迫性较低,与有症状感染相比投入要少得多,因此,除隔离观察外,只能考虑抗病毒干预。然而,对无症状感染者的治疗仍存在争议。尽管人们普遍认为抗病毒药物可以加快无症状感染的病毒清除5,23,但最近的几项研究表明,这些药物在加速病毒清除或症状改善方面作用有限,甚至无效24,25。
中国最早的医学典籍《黄帝内经》中记录,中医用于预防和治疗瘟疫,也被称为流行病。近年来,越来越多的循证研究证实了中医药治疗疟疾26、SARS27、甲型H1N1流感等传染病的有效性和安全性28。在抗击 COVID-19新冠肺炎疫情的斗争中,中医药在救治患者中发挥了重要作用。越来越多的证据表明,中医早期干预有助于提高临床治愈率,缓解症状,降低死亡率,有利于 COVID-19 患者的预后9,11,29。连花清瘟胶囊是中国政府权威机构推荐的一种广泛应用的治疗传染病的中药,于2015年获美国FDA批准进入II期临床试验。
一份关于COVID-19流行早期的报告显示,连花清瘟胶囊可改善轻、普通型COVID-19患者的临床症状13。考虑到无症状患者缺乏治疗药物和方法,作者还研究了连花清瘟胶囊对这些患者的疗效和对病毒的阻断效果,结果提示连花清瘟可以通过提高隔离观察期间核酸转阴的速率和缩短核酸转阴时间来加快病毒清除。这对无症状患者来说是一种重要的抗病毒作用,可能有助于延缓和阻断疾病进展。事实上,有报道称连花清瘟胶囊可以阻断SARS-CoV-2与ACE2的结合,抑制病毒复制,减少感染细胞中的病毒粒子30,31。
此外,我们的数据显示,连花清瘟治疗可减少临床症状的发生,最终降低无症状患者转为确诊轻症和普通病例的比例。近期的机制研究为连花清瘟胶囊及其活性成分可能与AKT1、IL-6、PTGS2、MAPK1等炎症反应和组织损伤的几个关键靶点结合提供了更多的科学证据32-34。这些数据解释了通过连花清瘟治疗,如何减少无症状患者的发热、肺部炎症和组织损伤的出现。连花清瘟胶囊在临床使用中的安全性是毋庸置疑的,因为本研究和许多其他试验很少或没有不良事件的报导10,13,35。
目前,COVID-19 的流行正在冲击我们的公共卫生,未来还将持续影响社会。无症状感染者是新冠病毒传播的关键环节,比例高,且传染性强。现阶段的干预措施相当有限。在本研究中,作者揭示了连花清瘟胶囊对无症状新型冠状病毒(COVID-19)感染患者可能的有益作用,可以考虑选择作为一种潜在的治疗手段。然而,这项研究存在一些局限性,本次试验规模较小,未实施安慰剂,可能影响结论的科学性。此外,由于缺乏对COVID-19无症状感染者的研究,本研究样本量的计算是基于临床经验。随着对 COVID-19 感染的了解不断加深,需要进一步研究连花清瘟胶囊对无症状COVID-19患者的作用。
致谢
统计分析由华中科技大学同济医学院公共卫生学院进行。
作者的贡献
QL、JM 和 SW 设计了试验并提供了行政支持。LZ、LW、XX、YY、RJ、XY、XZ、YG、HS提供研究资料,收集患者信息。LZ、LW、XX、JH 和 XW 分析并解释了患者数据。LZ、LW 和 XX 是撰写本文的主要贡献者。所有作者都阅读并批准了最后的文章。
出版同意书
计算机断层扫描表现图像的发表得到患者的同意。书面知情同意书由患者本人签署。
数据和材料的可用性
当前研究期间使用和/或分析的数据集可根据合理要求从相应作者处获得。
作者披露声明
作者声明他们没有相互竞争的利益。
资金信息
本研究得到国家自然科学基金重点项目(批准号:82130123)、河北省科技计划(批准号:206Z2503G)和国家重大科技专项(批准号:2017ZX10305501)的资助。
发表评论
最新评论

-

new凝心聚力谋发展 专业赋能启新程 | 2025年四川省居民健康素养监测工作研讨会在什邡圆满落幕
2025-05-09 -

new“国家应急医学研究中心西北基地”“甘肃省应急医院”落地甘肃省人民医院
2025-05-09 -

new第五届中国减重代谢手术视频比赛即将启幕 | 五大赛区联动赋能青年医师成长
2025-05-09 -

new祝贺!四川省肿瘤医院林桐榆教授、洪煌明教授团队领衔中国原研EZH1/2抑制剂HH2853实现r/r PTCL治疗新突破!
2025-05-09
-

摄影故事征集 | 将心内科的瞬间温暖绽放
2020-12-01 -

规范管理,推进实施——中国VTE防治大会暨全国肺栓塞和深静脉血栓形成防治能力建设项目年度进展工作会议在北京召开
2019-10-22 -

雄安论坛|图片花絮②
2018-11-19 -

雄安论坛 图片花絮
2018-11-14
-

e路有你 联抗慢病丨2021互联网慢病管理大赛收官
2021-09-24 -

福建:龙岩市第一医院3名最美逆行者出征!请平安归来!
2020-01-26 -

规范管理,推进实施——中国VTE防治大会暨全国肺栓塞和深静脉血栓形成防治能力建设项目年度进展工作会议在北京召开
2019-10-22 -

七旬老人千里求医终见光明
2025-05-06 -

中华医学会检验分会最新发布:有效生物安全防护指南--2019新型冠状病毒肺炎临床实验室检测(试行第一版)
2020-01-30 -
新冠疫情下的“影像幻影”——放射技师一线战斗纪实
2020-02-24 -

2020姑息大会开幕|凝心聚力,推动中国支持与康复诊疗事业勇攀高峰
2020-10-20






