经导管主动脉瓣置换术十大要点
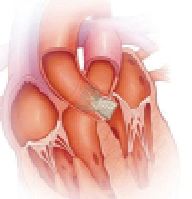
严重主动脉狭窄患者常合并多种并发症,常影响医生的治疗决策。近年来,经导管主动脉瓣置换术(TAVR)相关研究取得了诸多重要进展。3月22日,《美国心脏病学学院杂志》发文总结了这些进展,并对TAVR的未来发展与挑战进行展望。以下为其中的10大要点。(J Am Coll Cardiol.2016,67:1472)
1,TAVR已成为治疗严重主动脉狭窄(AS)的一种安全有效的手段。
2,近期研究发现,对于风险相似的患者,新一代TAVR装置与外科手术治疗后的血液动力学表现与临床预后相当,甚至优于后者。
3,基于当前临床证据,美国心脏学会(AHA)/美国心脏病学学院(ACC)指南已将TAVR列为严重症状性AS患者(I级推荐)治疗手段,预期生存时间1年以上。
4,对于外科手术瓣膜置换术后死亡或并发症风险较高的严重症状性AS患者,现行指南也推荐其选择TAVR治疗(IIa级推荐)。
5,很多最初不适合应用TAVR治疗的问题已得以解决,包括频发入路并发症问题,以及对卒中和瓣周漏风险的担忧。
6,组建多学科心脏治疗团队能够优化患者筛选、手术计划及装置置入等问题,可较为准确地预测患者临床预后。ACC/AHA指南及欧洲心脏学会指南均推荐,完成TAVR手术需要常规的心脏瓣膜团队(I级推荐)。
7,在当前的TAVR治疗时代,TAVR设计的加强提高了瓣膜置入时的稳定性,新型球囊扩张式装置使导入系统可回收及可复位,这两方面极大改善了瓣膜置入的精确性。
8,未来的研究应关注TAVR的耐用性,进一步改善临床结果以及辅助治疗方面。未来的TAVR应包括更小的外形(适合所有股动脉途径的TAVR患者),改进设计和技术,例如组织工程学心脏瓣膜。
9,基于部分临床试验的初步结果,未来TAVR似乎能够用于低危患者。
10,整体而言,TAVR技术已经改变临床实践,并将继续为AS患者的治疗作出重要贡献。
近年来,TAVR在我国也迅速发展,从2010年首例TAVR的完成,到国产Venus-A瓣膜注册研究完成,5年内我国学者在该项技术方面积累了初步经验。
此外,我国也于2015年12月发布了《经导管主动脉瓣置换术中国专家共识》,共识从TAVR的适应证和禁忌证、病情评估、硬件设施、人员及资质要求、手术操作要点、并发症的预防和处理、特殊情况的TAVR的处理等多方面进行了详细阐述。
适应证 共识指出,外科手术禁忌、预期寿命超过1年、症状性钙化性重度AS是TAVRⅠ类适应证,外科手术高危、预期寿命超过1年、症状性钙化性重度AS是ⅡA类适应证。外科手术禁忌是指预期术后30 d内发生死亡或不可逆合并症的风险>50%。外科手术高危主要是指美国胸外科医师协会(STS)评分≥8分者。
鉴于我国不同地域医疗发展水平不均衡,共识指出,对于外科手术高危、禁忌的认识与国外有别,在目前医疗环境及认知下,国内心外科手术患者选择趋向于保守。现阶段,对于外科手术高危和禁忌患者,建议由两位或两位以上心胸外科医师评估认定,STS评分作为参考。
禁忌证 TAVR的禁忌证包括:左心室内血栓、左心室流出道梗阻、30 d内心肌梗死、左室射血分数<20%、严重右心室功能不全、主动脉根部解剖形态不适合TAVR。
术前评估 包括临床评估及影像学评估。
临床评估包括:是否需要瓣膜置换术;是否为外科手术禁忌或高危;有无TAVR手术禁忌证。
共识指出,影像学评估是TAVR术前评估的重点,包括主动脉瓣膜、主动脉瓣环、升主动脉及外周动脉解剖情况,以判断是否适合TAVR及选择瓣膜的型号。
硬件设施、人员及资质要求 共识建议,TAVR在改装的心导管室或杂交手术室进行,并建议建立由心内科医师、心外科医师、超声心动图医师、放射科医师、麻醉师、护士及相关专业技术人员构的多学科心脏团队。
共识要求心外科医生在开展TAVR前的1年内,实施100例以上SAVR。心内科医生年介入手术量在200例以上,且接受过系统的培训。且在开展前20例TAVR应在有经验的手术医生协助下完成,之后可独立进行TAVR。此外,共识要求开展TAVR的中心必须有血管外科专科医生。
操作要点 共识建议,TAVR在静脉麻醉下、超声心动图及DSA引导下完成。共识以经股动脉置入自膨胀瓣膜为例阐述了TAVI的操作要点。包括血管入路的建立、导丝进入左心室、装载瓣膜、球囊扩张、释放瓣膜、退出CDS及缝合血管。
热点研究
高血压不是急性主动脉夹层
患者死亡危险因素
近期,中国医学科学院阜外医院张澍教授等研究显示,高血压是急性主动脉夹层(AAD)常见的合并症,Stanford B型AAD合并高血压比例较高。此外,合并高血压的AAD患者年龄较大,合并其他心血管病的比例较高,接受手术治疗的比例偏低。但高血压并非AAD患者长期或短期死亡的危险因素。(中华心血管病杂志.2016,44:220)
结果显示,合并高血压的AAD患者共733例,其中Stanford B型患者中合并高血压比例明显高于Stanford A型(71.3%与64.2%)。
此外,合并高血压的Stanford A型和B型患者年龄均较大,合并冠心病、糖尿病的比例相对较高,接受手术治疗的比例较低(P均<0.05)。
Stanford A型患者中,合并高血压的患者住院病死率和长期病死率与不合并高血压的患者比较差异均无统计学意义。Stanford B型患者中,合并高血压的患者其住院病死率明显高于不合并高血压的患者(5.4%与0.7%),但二者长期病死率差异无统计学意义。
多因素回归分析结果显示,高血压不是AAD患者住院死亡的危险因素。对于Stanford A型患者而言,手术治疗是住院死亡的保护因素;对于Stanford B型患者而言,年龄和手术治疗是住院死亡的独立危险因素。
研究连续入选2008年1月至2010年12月在阜外医院就诊的AAD患者1087例。
冠脉钙化增加
多种非心血管病风险
冠脉钙化(CAC)可独立预测全因死亡,包括心血管病和某些非心血管病事件所致的死亡,但与非心血管疾病之间的因果关系尚未确定。
近期美国一项研究显示,CAC与多种年龄相关的慢性疾病独立相关,尽管其相关程度弱于心血管病。CAC>400时,癌症、慢性肾脏病、慢阻肺和髋部骨折风险增加。(JACC Cardiovasc Imaging.2016年3月3日在线版)
研究纳入6814例受试者,中位随访10.2年。校正多种混杂因素后显示,与CAC = 0的受试者相比,CAC >400的受试者其癌症 (HR=1.97)、慢性肾脏病 (HR=1.7)、肺炎(HR=1.97)、慢阻肺(HR=2.71)和髋部骨折(HR= 4.29)风险均增加。但深静脉血栓形成/肺栓塞和痴呆的风险未增加。
与CAC>0的受试者相比,CAC=0的受试者患癌症(HR=0.76)、慢性肾脏病(HR=0.77)、慢阻肺(HR= 0.61)和髋部骨折(HR= 0.31)的风险下降。但CAC=0并不意味肺炎、痴呆和深静脉血栓形成/肺栓塞风险下降。
虽在不考虑非致命性冠心病患者后,这些风险间的联系有所衰减,但仍具有统计学意义。

发表评论
最新评论

-
02-172025
八家学协会共同发布心脏置入式电子设备合理应用标准,用好心电设备 守护心律健康
-

new《妇科肿瘤免疫检查点抑制剂临床应用指南(2023版)》正式发布
2023-04-09 -
03-132023
2023年春季成人流行性感冒中医药防治专家共识
【编者按】 自 2023 年春季以来,流行性感冒发病在我国各地呈上升趋势,本病属于中医“疫病”“时行感冒”范畴,中医药在减轻、消除流感症状、缩短病程方面疗效显著,为有效防治当前春
-

newCACA技术指南精读巡讲
2023-02-13
-

CACA技术指南精读巡讲
2023-02-13 -

《晚期非小细胞肺癌抗血管生成药物治疗中国专家共识(2019版)》发布
2019-07-26 -

简单路径 打通高血压指南实施最后一公里
2019-02-21 -

全程管理 让艾滋病患者在有效治疗下长期、有质量生存
2018-12-23 -

《中国脑卒中防治报告2018》解读
2018-11-13
-
2023年春季成人流行性感冒中医药防治专家共识
2023-03-13 -

《妇科肿瘤免疫检查点抑制剂临床应用指南(2023版)》正式发布
2023-04-09 -
【指南与共识】女性慢性心力衰竭管理的中国专家共识
2022-08-02 -

CACA技术指南精读巡讲
2023-02-13 -

良性前列腺增生指南权威解读:重视全病程管理,让指南走向基层服务临床!
2022-06-25 -

重磅!9部全国肿瘤放疗质控指南在深发布(附指南下载地址)
2021-12-27 -

《中国脑卒中防治报告2018》解读
2018-11-13







