打造呼吸科肺癌精准诊疗第一线 (上接第22版)



精准诊断第一线
从临床视角看 NSCLC分子标志物进展
▲ 河北医科大学第四医院 丁翠敏
目前,临床应用的个体化靶向治疗主要针对EGFR基因突变阳性和ALK融合阳性肺癌。随着对驱动基因的深入研究及少见驱动基因的发现,临床医生也真正从基因水平认识到了肺癌的复杂性。
驱动基因检测已成为日常临床实践
2015年,WCLC报道了亚洲及俄罗斯晚期非小细胞肺癌区域诊断实践(IGNITE研究)。结果表明,亚太地区的驱动基因检测的标本,主要来源于肺部原发病灶、淋巴结、胸腔积液。标本获取方式主要包括细胞学检测、支气管镜、细针穿刺、影像学引导下的穿刺活检。
绝大多数标本中肿瘤细胞含量超过20%,足以进行基因检测。在多渠道多途径提供充足的标本情况下,驱动基因检测的成功率高达99.5%,表明对于新确诊的局部晚期及转移性NSCLC进行驱动基因检测已成为日常临床实践。
MET突变有望成为靶向治疗的潜在靶点
2014年7月,美国癌症基因研究组通过对mRNA和DNA高通量测序结果及序列比对分析发现,约4%肺腺癌存在MET第14外显子(MET exon14)剪接位点突变,导致MET exon14在mRNA水平出现部分或完全跳跃缺失(MET exon14-skipping)。
2015年5月,在《肿瘤发现》同一期发表了两篇报道,Paik等在178例Ⅳ期肺腺癌中发现8例MET exon14缺失,4例患者接受克唑替尼或卡博替尼,1例完全缓解和3例部分缓解。Frampton等在38 028例肿瘤中发现了224例MET exon14缺失,其中发生率较高的癌症依次为肺腺癌、其他肺肿瘤、脑胶质瘤、及原发灶不明癌。MET exon14胸部组织细胞肉瘤及 MET exon14 NSCLC对MET 抑制剂敏感(图1、图2)。
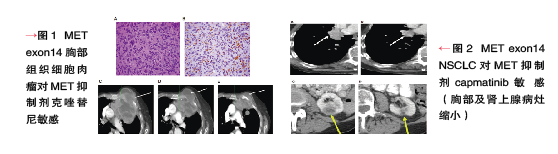
肺肉瘤样癌(PSC)是一种预后较差的高度侵袭性癌。为制定该肿瘤的新型治疗策略,需进一步了解其分子病理机制。 中山大学刘学文教授等对此进行了研究, 细胞实验证实,应用MET抑制剂能有效抑制MET exon14-skipped介导的下游信号激活和突变肿瘤细胞的生长、增殖。同时报道了1例肺肉瘤样癌接受克唑替尼治疗肿瘤退缩约80%。这8例MET exon14突变患者的特征为不存在EGFR、KRAS、BRAF、ALK突变(互斥)。其中1例合并有PIK3CA突变。在8例MET突变中,7例的肿瘤组织存在腺泡样腺癌成分。
MET exon14突变可能是NSCLC的一种独特临床亚型。美国Dana-Farber癌症研究所Mark M. Awad等报告,NSCLC中MET exon14突变与高龄、分期相关的MET基因组扩增以及c-MET过表达有关。因此,有必要开展前瞻性临床研究以验证MET exon14突变是否为NSCLC的一个重要治疗靶点。
从2014年7月,TCGA发现肺腺癌MET exon14-skipping到现在,在近2年就MET exon14-skipping发表的的研究已超过10项,MET抑制剂显示了极好的近期疗效,从而引起人们的极大兴趣和研究热情。MET突变可能有望成为其靶向治疗的潜在靶点。
液态活检:肺癌精准治疗之基石
▲ 第四军医大学第一附属医院 张艰
随着分子生物学的发展,精准医学在不断推进,肺癌特别是NSCLC治疗从以含铂化疗为主逐渐转变为以基因检测为基础的靶向治疗。基因分型、疗效评估、耐药监测成为肺癌靶向治疗的三部曲,而活检风险、组织不合格、患者无法耐受、肿瘤本身的异质性均使组织替代品应运而生,即“液态活检(CTC)”。
检测方法 CTC包括富集技术与检测技术,富集技术多数是根据CTC的生物学特性与化学特性进行富集。包括膜过滤法、免疫磁珠分离法、微流体芯片法等。CTC检测技术集中在靶向PCR、免疫荧光、普通PCR。CellSearch系统为首个被FDA与cFDA同时注册的CTC检测方法,一直是CTC检测的金标准。2016年1月中国自主研发的CytoploRare系统成为CFDA唯一认证的国内自主研发的CTC检测方法,不同分期肿瘤CTC检测的平均敏感度达80%,是目前敏感度最高的检测方法,希望能在临床上广泛应用,服务于肺癌的个体化治疗。由于ctDNA 含量少、片段短、半衰期短的特性,其检测方法要求较高,高敏感度的数字PCR及高通量的下一代测序成为血浆检测热点。
临床应用 包括肺癌的辅助诊断,与影像学及已知的肿瘤标记物共同诊断疾病;肺癌的复发监测,对早期术后肺癌行复发监测;.晚期肺癌行基因分型及疗效评估;靶向治疗耐药监测。
未来发展 CTC与ctDNA 均可即时、无创监测肿瘤发生发展及耐药突变,期待其能够更早、更全面地指导临床实践,更好地推进肺癌的个体化治疗。另外,CTC检测的是肿瘤细胞,ctDNA检测肿瘤DNA片段,细胞能提供比DNA片段更多的信息,两者的结合会提供更全面的肿瘤信息,真正实现精准医疗。
肺癌早期诊断支气管镜检查必不可少
▲ 广东省人民医院 高平
2013年中国肿瘤年报显示,肺癌发病率、死亡率排名第一。肺癌5年生存率约15.6%,75%患者在诊断时已属晚期。因此,肺癌早期诊断尤为重要。
肺癌病理可通过痰检、支气管镜、经皮肺内病灶穿刺针吸活检术(TFNA)等方法获得。与TFNA相比,支气管镜检查时气胸发生概率仅为1%,安全性高。
支气管镜检查已成为临床肺癌诊疗必不可少的技术。支气管镜下可分为可见病灶(多为中央型肺癌)和不可见的病变(外周病灶或管壁外病灶)。
可见病灶诊断手段
光干涉断层扫描 与支气管镜相结合,对支气管上皮、黏膜、软骨和腺体的细微图像显示清晰,与组织学检查吻合率极高。
自荧光支气管镜 在自荧光显微镜下,正常黏膜显示为绿色,而病变组织表现为紫红色或红褐色。
窄带成像支气管镜 是一种新型内镜成像技术,蓝色窄谱光,波长为390~445 nm,可显示黏膜表面的毛细血管;绿色窄谱光,波长为530~550 nm,可显示黏膜内较粗的血管。NBI可增强黏膜的对比度和清晰度,强调黏膜血管形态及表面结构,对于血管发生异常的肿瘤组织具有“电子染色”的作用。
支气管成像技术在判断肿瘤边界方面有更高的敏感性和特异性。
不可见病变诊断手段
虚拟支气管镜导航技术 通过CT重建虚拟支气管图像,并指示出到达病变的路径。其优势在于确认支气管镜行进方向,引导支气管镜到达所指定的病变部位,把握支气管镜当前位置,减少不必要的透视。
电磁导航技术 通过电磁感应原理进行定位。先行CT检查并将图像信息输入到计算机中,这类似于GPS电子地图;活检钳或治疗器具头端安装有电磁导航线圈,通过感应线圈可感应到其在磁场中的位置,其作用类似于GPS信号接收器。
引导鞘气道内超声(EBUS-GS) 超声探头可通过支气管镜进入镜下不可见的支气管,利用超声确认病变,然后留置引导鞘,放入活检钳和细胞刷获取病理标本。EBUS-GS结合X线透视、虚拟支气管镜技术、电磁导航技术可进一步提高病变的检出率。
气道内超声技术 对肺门淋巴结的转移病变的诊断上优于胸部CT,并可以实时指引穿刺活检;EBUS-TBNA该操作属于微创操作,可获得第2、4、7、10~12站淋巴结,肺癌联盟最新指南中已将EBUS-TBNA技术列为肺癌分期手段的第一位;对气管支气管壁层次的分辨可作一般病变和癌前病变的诊断;对肺外周良、恶性病变的评估,实时指导穿刺活检;指导气道内介入治疗。
肺癌特征
★边界清晰的低回声团块影;
★ 内部回声不均匀;
★ 内部见点线状高回声;
★病灶内部血管或支气管狭窄或中断;
★支气管软骨移位、不规则或中断;
★ 邻近血管狭窄或中断。

发表评论
最新评论

-
02-172025
八家学协会共同发布心脏置入式电子设备合理应用标准,用好心电设备 守护心律健康
-

new《妇科肿瘤免疫检查点抑制剂临床应用指南(2023版)》正式发布
2023-04-09 -
03-132023
2023年春季成人流行性感冒中医药防治专家共识
【编者按】 自 2023 年春季以来,流行性感冒发病在我国各地呈上升趋势,本病属于中医“疫病”“时行感冒”范畴,中医药在减轻、消除流感症状、缩短病程方面疗效显著,为有效防治当前春
-

newCACA技术指南精读巡讲
2023-02-13
-

CACA技术指南精读巡讲
2023-02-13 -

《晚期非小细胞肺癌抗血管生成药物治疗中国专家共识(2019版)》发布
2019-07-26 -

简单路径 打通高血压指南实施最后一公里
2019-02-21 -

全程管理 让艾滋病患者在有效治疗下长期、有质量生存
2018-12-23 -

《中国脑卒中防治报告2018》解读
2018-11-13
-
2023年春季成人流行性感冒中医药防治专家共识
2023-03-13 -

《妇科肿瘤免疫检查点抑制剂临床应用指南(2023版)》正式发布
2023-04-09 -
【指南与共识】女性慢性心力衰竭管理的中国专家共识
2022-08-02 -

CACA技术指南精读巡讲
2023-02-13 -

良性前列腺增生指南权威解读:重视全病程管理,让指南走向基层服务临床!
2022-06-25 -

重磅!9部全国肿瘤放疗质控指南在深发布(附指南下载地址)
2021-12-27 -

《中国脑卒中防治报告2018》解读
2018-11-13







