药源性疾病:安全之殇
编者按:药物在改变疾病处理方式的同时,其安全性问题已成为医疗中难以消除的隐患,反过来威胁着人类健康。5月23-24日在京召开的“第六届药源性疾病与安全用药中国论坛-消化系统与肝病药物专题研讨会”上,来自国内外相关领域临床和药学专家就药物所致消化和肝脏疾病的循证医学、风险管理、肝损伤机制及预防方法进行了交流讨论。此外,会上成立了中国药理学会药源性疾病学专业委员会,原首都医科大学宣武医院药剂科主任王育琴教授担任主任委员。

【药物性肝损伤与肝病药物合理应用】
药物性肝损伤是药物不良反应“重头戏”
药物性肝损伤(DILI)是最主要的药物不良反应之一。上海南京军区临床肝病研究中心陈成伟教授表示, DILI已引起药学、制药企业、药品管理部门及公众的重视,是药物审批失败、增加警示及撤市的主要原因。在美国,DILI超过其他病因总和,成为急性肝衰竭的首要原因。
药物、宿主基因型和环境共同决定DILI的发生。相关基因学研究包括药物代谢酶遗传多态性、肝脏转运蛋白基因变异、人类白细胞抗原遗传多态性等。环境因素包括免疫致敏、炎症、氧化应激、谷胱甘肽耗竭等。此外,线粒体损伤或功能障碍,致线粒体通透性改变,可造成肝细胞炎症、损伤,触发细胞凋亡和坏死。
1999年提出的Hy’s法则,即当药物性肝损伤出现丙氨酸转氨酶≥3×正常上限值(ULN)且总胆红素>2×ULN时,通常提示预后不良,是美国食品药品监督管理局新药研发评估中评价肝毒性的参考标准,也是众多医学和药学研究工作者信赖的医学判断准则之一。国际严重不良反应协会2011年发布标准化命名的国际共识,将丙氨酸转氨酶阈值提高到5×ULN,原因是低水平阈值会导致不必要的检查和不恰当的停药,调整后或可将不重要的自限性药物相关事件和脂肪性肝炎等排除。
近年来,我国在DILI领域进行了不少开创性工作,包括加强中草药与保健品肝毒性研究、建立半定量评分系统、探索适应性免疫攻击对DILI发生的作用等。
安徽医科大学第一附属医院徐建明教授介绍了一项我国肝窦阻塞综合征(SOS)多中心、回顾性调查(2010-2011年),结果显示,我国住院SOS患者的主要病因为中草药(66%~72%),其中以土三七最多见(35%~62%),提示有必要开展中草药吡咯类生物碱单体成分的毒理学研究。
陈成伟教授表示,药物基因学、氧化应激、线粒体损伤、新的生物标志物将是DILI今后的研究热点。药物性肝损伤网全球合作、新评估工具eDISH程序的推广应用将对DILI研究以及药物研发起巨大推动作用。
核苷(酸)类药物需关注肾脏-骨骼损害
安全性是慢性乙肝患者核苷(酸)类药物长期管理的关键因素之一。重庆医科大学附属第二医院院长任红教授指出,核苷(酸)类药物长期治疗的慢性乙肝患者可能出现肾脏损伤,要避免此类不良事件的发生,首先应识别潜在的肾毒性风险因素,如糖尿病、动脉粥样硬化和老年患者等。核苷(酸)类药物是慢性乙肝患者骨密度下降的独立影响因素之一。慢性乙肝抗病毒治疗过程中乳酸酸中毒与肝病严重程度相关,严重肝病患者使用核苷(酸)类药物时需关注潜在乳酸酸中毒风险。
北京地坛医院蔡晧东教授表示,替诺福韦是今年在我国上市的第5种抗乙型肝炎病毒的口服核苷(酸)类药物,也是迄今被认为抗病毒作用最强、耐药率最低的药物,但其潜在的肾脏-骨骼损害仍应引起重视。其肾损害发生机制与阿德福韦相似,包括在肾脏蓄积与高浓度、对肾小管线粒体毒性、肾小管转运蛋白存在遗传性功能缺陷。替诺福韦可导致骨密度降低、骨质疏松,甚至发生骨折。主要机制为替诺福韦的肾小管损害导致低磷血症、低钙血症和肾小管性酸中毒,继发性导致骨破坏增加,骨合成减少,骨密度降低;此外,替诺福韦对骨组织的直接毒性,造成骨细胞线粒体DNA合成障碍。为此,蔡晧东教授表示,替诺福韦治疗过程中应定期监测血磷和血清肌酐水平;发现肾脏-骨骼毒性及时处理,包括改变治疗方案、调整药物剂量、补磷,急性肾衰竭者可透析治疗;补充维生素D、辅酶Q10等。
【药源性消化系疾病】
药物性胰腺炎多以急性为主
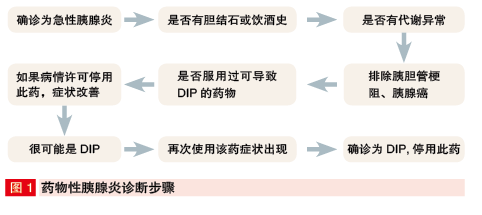
药物性胰腺炎(DIP)是指某些药物导致胰腺分泌功能或胰腺组织器官损害,其临床表现为急性胰腺炎的症状及体征。北京朝阳医院药剂科刘丽宏教授指出,DIP一直被认为是相对少见的疾病,至今无确切发病率统计。有研究估计,DIP约占全部急性胰腺炎的0.1%~2%。抗生素、抗人获得性免疫缺陷病毒药、利尿剂、消化系药物、心脏疾病药物、免疫抑制剂或化疗药、神经精神药物等均可导致DIP。DIP的发病机制包括直接毒性作用、免疫反应或过敏反应、高血压或高血钙、奥迪括约肌收缩或胆管阻塞、胰管阻塞或胰液排泄不畅。
同其他原因引起的胰腺炎一样,DIP也常以腹痛为首发症状或主要表现。由于没有独特的临床表现,DIP的诊断常具有挑战性。刘丽宏教授介绍,2011年一项发表在《美国胃肠病学杂志》的文章建议,对于原因不明的急性胰腺炎患者,医生应更多的想到DIP的可能性,并采取适当措施,停止使用相关药物。
北京协和医院消化内科钱家鸣教授表示,激发试验阳性有助于DIP诊断,DIP较少表现为慢性胰腺炎,最常见为轻度胰腺炎,预后良好。但也有重度胰腺炎甚至病情危重导致死亡的报道,临床仍需重视其诊断(图1)。
合理联用质子泵抑制剂
减少抗栓治疗所致胃肠出血
应用传统非甾体类抗炎药(NSAID)患者,2%~4%可有明显胃肠道并发症;1%~8%的患者开始用药1年内因消化性溃疡住院;约20%长期用药者可出现消化性溃疡。上海交通大学医学院附属瑞金医院消化科袁耀宗教授介绍,消化道损伤高危人群包括65岁以上老年人、有消化道出血/溃疡史、有消化不良或胃食管反流症状、双联抗血小板治疗患者/合用华法林等抗凝药物患者、合用NSAID或糖皮质激素患者、幽门螺杆菌(Hp)感染、吸烟、饮酒等。抑酸治疗可降低阿司匹林的胃肠道不良反应,H2受体拮抗剂预防阿司匹林相关胃肠道并发症证据较少,疗效优于安慰剂。Meta分析显示,大剂量静脉使用质子泵抑制剂(PPI)可降低再出血发生率、再次内镜检查率、手术率、输血率和死亡率。抗血小板药物消化道不良反应处理原则:是否停药需权衡患者血栓和出血风险;不建议氯吡格雷替代阿司匹林治疗,建议阿司匹林联合PPI;积极给予抑酸药和胃黏膜保护剂,首选PPI,并根除Hp,必要时输血。
北京大学第三医院消化科周丽雅教授表示,与单用阿司匹林相比,阿司匹林联合氯吡格雷抗栓治疗增加上消化道出血率。双联抗血小板治疗时,如需合用PPI,建议连续使用不超过6个月,此后可换H2受体拮抗剂或间断使用PPI。服用氯吡格雷患者需联合使用PPI时,应尽量避免使用奥美拉唑及埃索美拉唑。心血管高危者使用阿司匹林如发生出血应立即停止使用,但溃疡出血经内镜下成功止血后3~5 d,应尽快恢复阿司匹林使用。

发表评论
最新评论

-
04-292025
高危膀胱癌患者联合治疗方案有新突破
-
04-262025
晚期黑色素瘤一线免疫疗法有新方案
-
04-252025
晚期肾癌一线靶免联合治疗有新方案,推动临床治疗格局变革
-

new“健康体重 医者先行”主题推进活动在京举行
体重管理工作体现了“以治病为中心”向“以人民健康为中心”的转变
2025-04-23
-

独辟蹊径!易俊林团队发现缩小鼻咽癌患者放疗靶区新方法
2024-03-10 -

《2023中国高脂血症诊疗现状与疾病管理调研报告》在第六届进博会发布
2023-11-07 -

传承百年创新征程,攻坚糖尿病未竟之业
2023-04-12 -
18厘米超长阑尾被保住!《胃肠内镜》刊登我国专家保阑尾ERAT治愈最长阑尾急腹症病例
2022-12-11 -

泛肿瘤TRK抑制剂罗圣全®在中国获批,开启个体化医疗新篇章
2022-07-29
-

聚焦世界脑健康日五大核心目标,携手同行共促脑健康,2023中国脑健康大会成功举办
2023-07-27 -

18厘米超长阑尾被保住!《胃肠内镜》刊登我国专家保阑尾ERAT治愈最长阑尾急腹症病例
2022-12-11 -

全球首部钙调磷酸酶抑制剂治疗风湿免疫性疾病临床应用专家共识全国发布
2023-06-12 -

县域医疗机构消化专科精准能力提升项目湖南试点启动会在长沙召开
2023-05-30 -
【5·11世界防治肥胖日】今天,大声喊出“我要瘦”!
2016-05-17 -

两院院士增选工作正式启动!医学领域儿科、麻醉、神经病学优先增选推荐!
2023-07-27 -

长期肥胖增加食管癌和贲门癌风险
2017-08-06






