干细胞临床研究 非三甲医院不要涉及
本报讯(记者 杨萍 宋攀)近日,国家卫生计生委、国家食品药品监督管理总局联合发布《干细胞临床研究管理办法(试行)》(以下简称《办法》),旨在规范干细胞临床研究行为,保障受试者权益,促进干细胞研究健康发展。据悉,这是我国首个针对干细胞临床研究进行管理的规范性文件。
以干细胞治疗为代表的生物治疗已经成为二十一世纪最具活力的疾病治疗手段。据中国科学院院士吴祖泽介绍,目前,我国很多院校都在开展干细胞研究工作,多项研究成果在国际高水平杂志发表。2013年的一项数据统计显示,我国在干细胞领域发表的论文数量居世界第五位,仅次于美国、德国、日本、英国。然而,干细胞的临床研究、临床应用和产业化,还存在不少问题。
《办法》明确,从事干细胞临床研究的医疗机构必须具备三级甲等医院、药物临床试验机构资质和干细胞临床研究相关条件,医疗机构不得向受试者收取相关费用,不得发布或变相发布广告。根据规定,临床研究人员必须尽告知义务,由受试者签署知情同意书。对风险较高的项目,研究机构应当采取有效措施进行重点监管,并通过购买第三方保险,对于发生与研究相关的损害进行补偿。干细胞临床研究结束后,应当对受试者进行长期随访监测。
《办法》强调,此规定不适用于已有成熟技术规范的造血干细胞移植,以及按药品申报的干细胞临床试验。

责任编辑:
发表评论
最新评论

相关文章推荐
-

new创新“数字中医+科学减重”模式,开辟健康管理新路径
2025-07-15 -
07-142025
深化中西医协同 络病理论破解慢病防治“时代命题”
-
07-132025
解锁睡眠健康密码:中西医结合诊疗为失眠抑郁等难题破局
-
07-132025
络病理论引领创新 中西医协同助力前列腺疾病治疗新突破
推荐阅读
-
深化中西医协同 络病理论破解慢病防治“时代命题”
2025-07-14 -
解锁睡眠健康密码:中西医结合诊疗为失眠抑郁等难题破局
2025-07-13 -
络病理论引领创新 中西医协同助力前列腺疾病治疗新突破
2025-07-13 -

质量控制 | 赣医大一附院成功举办2025年江西省超声诊断专业质量控制中心专题工作会
2025-07-07 -

提高质量 健康优先丨第三届江西省超声医学质量控制培训举办
2025-07-07
热门资讯
-

我国发现一例输入性寨卡病毒感染病例
2016-04-18 -
中期甲状腺癌也可以经口腔镜手术
2023-04-23 -

2023年度医界好书评审结果公示
2024-03-07 -
中国医师协会学术会务部招聘启事
2016-09-01 -

郑大附一院消化病院刘冰熔院长内镜治疗新技术受国际关注
2016-12-05 -

2017年医师资格考试四大变化
2017-07-28 -
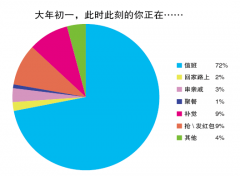
72% 坚守是他们的春节
2017-07-28






