艾伯维的2019
五大关键词盘点全球生物制药行业先锋企业艾伯维
推动前行的力量——十大医药先锋企业
光阴似箭,日月如梭,时序更替,梦想前行。站立2020年篇首,回望2019来路与脉络,国家主席 曾说,“一个流动的中国,充满了繁荣发展的活力。我们都在努力奔跑,我们都是追梦人。”
朝气蓬勃的全球生物制药行业先锋:艾伯维,在2019年充分展现了“标杆”的力量。接下来,就让我们以五个关键词盘点它的骄人2019。

关键词一: 快进
2019年5月,治疗丙肝的泛基因型产品艾诺全(格卡瑞韦哌仑他韦片)在中国获批上市;11月,修美乐®(阿达木单抗注射液)在中国获批第四个适应证——多关节型幼年特发性关节炎;血液肿瘤创新药物Venetoclax已在中国提交上市申请……预计,到2024年,全球排名前十的生物制药公司艾伯维将在中国上市10个新产品,涵盖30个新适应证。艾伯维创新药按下了进入中国的“快进键”。伴随“健康中国2030”大幕的拉开,艾伯维在中国的发展也将进入全新阶段。
艾伯维高层点评:艾伯维全球高级副总裁(负责日本、澳大利亚及新兴市场)Alberto Colzi:艾伯维见证了中国政府对全民健康的承诺,很高兴看到中国药监部门近年来加快了药品审评审批的速度,让更多的国外创新药更快地进入中国市场。目前,中国创新的宏观环境非常好,艾伯维在中国正专注于创新。Alberto Colzi指出,“艾伯维聚焦中国政府提出的健康中国2030目标,不遗余力地加快创新药物进入中国市场的工作力度,为‘健康中国2030规划纲要’的实现贡献力量,为推进中国健康事业发展而不懈努力,造福中国患者。”
关键词二 :医保
在不久前公布的完整版《国家基本医疗保险、工伤保险和生育保险药品目录》中,修美乐®的3个适应证——类风湿关节炎、强直性脊柱炎、银屑病被纳入其中,此举有望惠及更多中国患者。
修美乐®作为全球首个获批的全人源抗肿瘤坏死因子单克隆抗体,也是首款采用获诺贝尔化学奖的“噬菌体展示”技术生产的药物,已连续7年蝉联全球处方药销售排行榜第一位。
目前,修美乐®在全球拥有17个免疫介导炎症性疾病适应证,在中国获批的适应证有4个——类风湿关节炎、强直性脊柱炎、银屑病、多关节型幼年特发性关节炎。
艾伯维高层点评:艾伯维全球高级副总裁(负责日本、澳大利亚及新兴市场)Alberto Colzi:艾伯维是成立于2013年、朝气蓬勃的年轻公司,但艾伯维在业内有丰富积淀。修美乐®纳入医保只是艾伯维在风湿免疫领衔突围的一个成果;展望未来,艾伯维还将在免疫学、病毒学、肿瘤学和神经科学四大领域蓄势待发,还将带来更多足以改变治疗格局的革命性成果。
关键词三:临床急需
艾伯维的血液肿瘤创新药物Venetoclax已于2019年在中国提交上市申请。作为一种临床急需的救急救命药物,Venetoclax可用于治疗急性髓系白血病(AML)和慢性淋巴细胞白血病(CLL)。该药已在全球多个国家和地区获批。
统计数据显示,我国每年新增AML患者约4万人,存在未获满足的治疗需求。而AML是侵袭性非常高、进展很快的肿瘤类型之一,其患者5年生存率不足30%。特别是AML中75岁以上的患者,因为这类患者不适合接受强诱导的化疗方法,目前在中国无药可救。另外,Venetoclax能针对伴17p缺失的复发/难治型的CLL患者进行治疗。艾伯维希望Venetoclax能尽快来到中国,为临床上有迫切需求的患者带来生的希望。
艾伯维高层点评:艾伯维全球高级副总裁(负责日本、澳大利亚及新兴市场)Alberto Colzi:“中国政府非常重视对肿瘤患者的治疗,艾伯维也希望通过自身的创新技术造福更多中国肿瘤患者。在抗肿瘤领域,我们希望为中国患者带来更持久和优良的治疗手段。”
“Venetoclax目前在中国正在开展多项临床试验,我们希望加快推进各项工作。同时,我们也会积极探索其它的渠道希望能帮助中国患者,包括探索临床急需药品的加快审评审批的通道,特别是对于AML针对75岁以上的患者,因为这类患者不适合接受强诱导的化疗方法。”
关键词四:与全球同步
2019年,艾伯维全球研发副总裁兼首席医疗官Rob Scott两次来中国市场考察。与以往不同的是,这次他率领着研发团队的15位管理人员一同前来——“我想让大家亲身体会中国市场的变化,更好地了解市场的情况”。
艾伯维对中国市场的最终目标是,使其与全球市场同步,成为艾伯维全球研发和临床事业的常规组成部分之一,从而让艾伯维的创新药物能在中国与全球同步上市,满足中国患者的“未尽之需”。
艾伯维的研发团队对原有的研发策略和方式进行了革新,并取得了实际成果。日本已成为SkyriziTM(Risankizumab)药物全球上市的第一个国家。艾伯维希望能在中国复制这一成功。
艾伯维高层点评:艾伯维全球研发副总裁兼首席医疗官Rob Scott:艾伯维将新的研发策略及数字化(人工智能、大数据等)手段应用于日本,使其成为SkyriziTM全球首个获批的市场。我们希望将这一成功经验复制到中国市场,将中国纳入艾伯维的全球临床Ⅰ期、Ⅱ期和Ⅲ期研究规划。
目前,艾伯维已推出60多项数字化临床研发项目。进行数字化临床试验探索的最大挑战是打破固有理念。中国对很多新技术的应用已走在世界前列,但要真正实现数字化临床试验,关键在于让科研人员跳出原有思维框架,将新的技术与解决方案真正运用到临床试验中来。
关键词五:员工第一
2019年,艾伯维连续6年在中国获得“杰出雇主”的称号,这体现了艾伯维对员工的重视,从而也驱动了艾伯维在中国取得突出的成就。
艾伯维在中国发展的7年均取得了稳定的增长。在中国,艾伯维的创新基因与业务驱动模式,与中国政府鼓励创新的政策和锐意改革的行动一脉相承。
中国医改及“健康中国2030”正在给包括艾伯维在内的全球企业释放巨大的市场机遇!
艾伯维高层点评:艾伯维中国区总经理欧思朗:拥抱“中国机遇”,艾伯维在中国的发展已装上了“高速引擎”。一方面,我们将秉承 “以患者为核心”的内核,加速我们产品在中国市场的发展和上市速度,从而让更多的中国患者获益;另一方面,我们将坚持“员工第一”的理念,在企业内部建立高效、致胜的氛围,在不断加速引入更多卓越本土人才的同时,也让所有员工能快速成长,在工作驱动力下,建立快速、高效和创新的文化。
我们致力于在中国成为一家最值得信赖的生物制药公司,拥有共同梦想的我们,为患者提供创新的医疗方案,为员工提供优质的工作与成长环境,关爱生命,创造奇迹。
我们期待与中国携手,为“健康中国2030”、为彼此共同的健康目标奋进。
发表评论
最新评论

-

new杨一红:急诊科院前院内衔接 打通生命“最后一公里” | 高端访谈
急救的每一分钟都关乎生死,我们要用科技打通生命通道的“最后一公里”。
2025-05-13 -

new潘曙明教授:完善法律 保障医患共同权益 | 高端访谈
潘曙明教授深入剖析了急诊医学面临的伦理法律挑战及学科未来发展路径。
2025-05-13 -

new燕宪亮教授:急诊医学人才培养的破局之道 | 高端访谈
燕宪亮教授深入剖析当前急诊医学人才培养的现状、挑战与创新实践。
2025-05-13 -

new【现场直击】又一例!视频急救指导成功!
2025-05-12
-

叶军:从事临床医学教育教学43年的4点感悟
2025-01-06 -

医师报在进博 | 跟着医师报小分队,感受科技赋予健康的魅力!
2024-11-06 -

冬季哮喘、慢阻肺患者该如何预防?朱玉龙:确保病情得到有效的控制是关键
2023-12-18 -
全国肿瘤宣传周:癌症防治 “三全”在行动——专家倡导抗癌从治病向防治管理转变
2023-04-10 -
世界肥胖日丨糖胖病:要控糖,先治胖
2023-03-03
-
朱玉龙:肺部下叶小结节的活检诊断策略分享
2023-06-14 -

儿童意外伤害可防可控,国家儿童医学中心儿童意外伤害中心成立!
2023-07-19 -

中国大型创新型药物真实世界研究即将启动,研究成果将惠及更多中国特应性皮炎患者
2023-07-17 -

仁济医院吴文广教授:引领国内ERCP发展潮流
2022-11-08 -
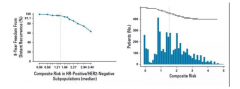
TEXT/SOFT研究报道8年无远处复发生存风险
2020-09-17 -

中国人民解放军总医院刘又宁: 讲好中国抗疫故事——重温我对新型冠状病毒感染的一己之见
2023-08-01 -
世界肥胖日丨糖胖病:要控糖,先治胖
2023-03-03






