准确发挥核酸检测在新冠疫情防控中的作用
本文作者:北京大学人民医院呼吸科 何权瀛
2019年末到2020年初暴发的新冠疫情是有史以来涉及面最广,持续时间最长,危害最大的一次流行病,它不仅在政治、经济、交通、旅游和文化领域,同时在人类健康和疾病领域均造成不可估量的损失。新冠病毒核酸检测是新冠疫情防控中最重要的环节之一,然而最近的实践表明新冠病毒核酸检测尚存在某些问题,特别是假阴性问题。本文将围绕病毒核酸检测(下简称核酸检测)当中存在的若干问题及改进措施进行简要讨论。
一、病毒核酸检测的重大意义和作用
目前认为病毒核酸检测至少在以下几个方面具有重大意义:
1.为寻找新冠病毒传染源,明确传播途径提供重要的,有时甚至是唯一的线索和证据。在疫情大面积流行时期,如2020年1-5月在我国武汉乃至湖北疫情暴发,以及后期区域性地流行,如2020年夏季北京新发地和2021年春天石家庄地区疫情局部暴发均是如此。目前我国处于“外防输入,内防反弹”的特殊历史时期,做好病毒核酸检测,仔细寻找传染源则是十分重要和关键的,通过病毒核酸检测,可以准确的评估输入风险,识别近期以及未来风险增加的迹象,为加强防疫工作最终战胜疫情提供帮助。[1]
在这个过程中,检测无症状感染者则具有十分特殊的意义。据某省未公开的数据显示,2020年3月13日累计报告病毒核酸阳性者290人,医学观察14天后176人(60.7%)转为确诊病例,114人(39.3%)为无症状感染者,又称为病毒携带者,截至同年3月24日,密切接触者中病毒核酸检测阳性者516人,其中449人(87%)转为确诊病例。67人(13%)为无症状病毒携带者。[2]如果没有准确的核酸检测,我们根本无法发现这些具有传染性的无症状感染者。高文静等对6项研究结果进行分析,指出30%-60%的新冠病毒感染者无症状或症状轻微[3],2020年3月23日,我国26个省份密切接触者健康检测数据显示,在1219例核酸检测阳性者中,隔离14天后仍有336人(27.56%)为无症状病毒携带者。[2]我国的研究结果显示,无症状感染者的密切接触者存在2代病例续发的危险,这也就是说,处在潜伏期,或病毒携带者也具有传染性,而且危害更大。[4、5]欲在人群中发现无症状感染者,重要的甚至是唯一的方法就是病毒核酸检测。
2.为临床诊断提供强有力的证据。我国历次制定的新型冠状病毒肺炎防治方案中,绝大多数均将核酸检测阳性作为新冠肺炎诊断的主要依据。这一点是完全必要和正确的,但是应当看到目前核酸检测中还存在一定的假阴性问题,这可能会影响到新冠肺炎临床诊断的准确性。
3.作为判断新冠肺炎是否符合出院标准。2020年我国第一版新冠肺炎诊治方案,直到今年第九版新冠肺炎诊治方案中,一直明确规定收治的新冠肺炎患者,出院标准中十分强调病毒核酸检测必须连续三次阴性才算符合出院标准,其用意则在于确定这些患者不仅病情完全稳定,而且不再具有传染性,为这些患者出院后的生活、工作、学习安排提供必要的依据。
二、目前我国新冠肺炎中核酸检测真实水平
2020年初武汉大学人民医院进行的一项横断面研究,从1月20号到2月9号,他们对该院就诊的8274例COVID-19疑似人群采用荧光定量PCR方法,检测标本包括呼吸道标本和非呼吸道标本。以核酸检测结果分组,ORF1ab和N基因同时阳性者判断为核酸检测阳性组,两者同时阴性归为阴性组,其中单一基因靶标阳性归为可疑组。结果显示,8274例受检者中,2745例(33.17%)核酸检测结果为阳性,5277例(63.77%)结果为阴性,252例(3.05%)结果为可疑。因为当时没有相应的抗体检测,因此难以判断核酸检测的敏感性和特异性。[6]由于那时我国病毒核酸检测处于疾病流行的早期,核酸诊断的效能未经大样本临床认证即用于临床,因此很早就有专家指出新冠病毒检测结果存在假阴性问题[7],由于新冠病毒核酸检测检测结果受到多种因素影响,包括标本的采集、标本的运输和实验室操作。据我们检索到的文献,后期病毒核酸检测的阳性率明显提高。如汪明等报告阳性率为33.2%[6],黎威等报告核酸检测阳性率51.1%[8]李园园等报告为57.4%[9],刘焱斌报告为54%[10],此后国内仍不断出现核酸检测假阴性的情况。总之,现有的数据表明,目前我国病毒核酸检测中一直存在假阴性问题,但是并没有引起足够的重视。
三、临床应用中核酸检测假阴性问题和假阳性问题,尤其是假阴性问题[7,11-13],这个问题与上面所说的核酸检测阴性不同。
据2020年1月30日人民日报报道,天津有一例确诊的新冠病毒肺炎患者,自1月25日到1月28日共进行3次核酸检测,结果均为阴性,但在1月30日第四次核酸检测时才呈阳性,前后检测结果的不同给患者的诊疗造成一定影响。[11]不仅在天津,其后在北京顺义地区也发生过类似现象。中日友好医院出现过三阴病例[7],杭州曾报道过一例患者7次核酸检测,前6次均为阴性,最后一次才为阳性,导致临床医生对核酸检测的价值产生质疑。[7]
另一种情况是,核酸检测先是阴性后转阳性,即所谓复阳问题,也引起大家的关注。据里进等报告,一例女性患者76岁因发热,咳嗽加重,呼吸困难,胸部CT显示双肺感染,因核酸检测阳性收入到该医院ICU,入院后连续两次核酸检测都是阴性,因病情好转,转入感染科继续治疗,但随后两次核酸检测又转成阳性,这种阳转阴,阴转阳的患者在他们收治的3000多例患者中并不少见。[7]据有关报道,广东省出院的新冠肺炎中,14%出现出院后复查核酸又转为阳性的情况[14],另据重庆市报道,他们报告了5例患者核酸复阳现象,而这5例患者同期抗体均呈阳性。这提示之前报告的核酸检测阴性是假阴性。[15]不管是上述哪种情况,核酸检测假阴性都会给新冠疫情防控带来很大的困难[16],容易使新冠病毒在人群中蔓延。
四、核酸检测中出现假阴性的原因分析[13,17]
目前无论是临床试验室还是疾病预防控制中心(CDC实验室)病毒核酸检测时普遍应用的是实时荧光RT-PCR方法,这种检测方法成熟可靠,已在常规检验和科研试验中被广泛应用。[18]但是,在评价检查结果和效率时应当客观地考虑到由于方法学特点,疾病发展过程标本采集、标本保存与运输、核酸提取、扩增体系、检测人员操作技术等都可能造成检测结果的假阴性或假阳性。
在被感染者中,检出病毒核酸需要同时满足以下四个条件:
(1)被感染者的细胞中含有一定数量的病毒,如果采集的标本中病毒数量低于一定界限,在核酸扩增检测体系中则无法检出,从这个意义上来说某些情况下,病毒核酸检测假阴性是无法完全避免的;
(2)采集标本时,必须采集到确实含有病毒的细胞;
(3)可靠的体外诊断试剂;
(4)规范的临床核酸检测试验条件(合理的分区,有能力的检测人员和严格的质量管理体系);
1.患者的病程与病情
大部分新冠肺炎患者的发病都会经历一个从无症状潜伏期到轻度症状或典型症状和最后痊愈,少部分患者会表现为严重症状甚至病危的过程[19],不同病程和不同病情患者体内病毒存在量可能不同。病人典型或病情危重时,阳性率可能高一些,病情轻,症状少或无症状时阳性率可能会低一些。因此临床上采集标本进行核酸检测可能为阳性结果,也可能为阴性结果,其实任何病原学检测都不能只根据一次阴性结果做出排除性诊断,更不能根据病毒核酸检测阴性而轻易排除临床上高度疑似新冠肺炎,尤其是在疫情高发地区和大面积流行期间。在病程的不同时期多次采集多种标本进行检测是十分必要的。
2.标本的采集部位问题
大量研究结果显示,从患者鼻咽部采样检测阳性率高于口咽部采样,来自于下呼吸道采集的痰液、肺泡灌洗液标本阳性率高于口、鼻咽部拭子。但是采集来自下呼吸道的痰液和肺泡灌洗液标本难度较大,而且容易引起交叉感染。为了提高检测阳性率,建议采集同一患者多部位标本合并进行检测,比如用口咽拭子、鼻咽拭子同时采集标本然后放到同一采集管中送检,对于有消化道症状的疑似患者还应采集粪便或肛拭子进行检测。
3.标本的采集方法
采样的准确性主要取决于实验室操作人员的水平和责任感,如果标本采集者操作不规范也会导致采样误差,如医护人员采样量不足或者刮取标本的位置不对或深度不够、时间不够,没有划取到带有病毒的标本,或样本中病毒量太少也会导致检测结果阴性。
4.标本的运输和保存
新冠病毒属于RNA病毒,很容易被来自试剂、耗材等外源性或细胞破坏后释放的内源性RNA酶降解,从而影响最后的检查结果。严格地讲,标本采集后应立即送到实验室尽快完成检测。标本在常温条件下放置时间过长也可能是造成检测结果假阴性的原因,所以目前建议,标本采集后至少在4个小时内完成检测,如果因为某些原因采集的标本不能及时送检应将标本置于4℃内放置24小时,24小时内不能检测的标本建议保存于-70℃的环境内保存,但应避免反复冻融。[20]
5.核酸的扩增
不同厂家试剂的研发是根据COVID-19核酸OFR1ab、N、E等基因的特异性序列设计的扩增探针,不同的厂家扩增试剂可分为1、2或3个靶标基因位点检测试剂,而包含有不同靶标基因位点的试剂检测敏感度、特异度不同[21-23],试剂中酶、金属离子等成分与质量的差异都会影响扩增的效率和最后检测结果。因此,不同厂家的试剂、核酸检测试剂盒的质量差异也会影响到检测结果。[24】为了提高检测的敏感性,多数试剂厂家选择病毒核酸序列中的两个或两个以上区域进行检测,OFR1ab、N、E区为常见检测区。
6.核酸扩增仪器
不同实验室用于病毒核酸检测仪器种类有所不同(包括PCR仪或核酸扩增仪),不同的设备对于检测过程中不同温度的控制精度,对荧光信号检测敏感度等不同,也可能导致检测结果的差异。需要强调的是试剂分析的敏感性是有极限的。此外,试剂反应条件、反应体系优化、核酸加入量都可能影响检测分析的敏感性。
7.病毒核酸的变异
随着疫情的进展,特别是病毒面临消毒、抗病毒治疗压力下,可能会产生基因位点核酸序列的变异,如果变异的位点处于核酸扩增的引物结合区,也可能出现假阴性结果。
8.患者用药情况对检测结果的影响
据报告,抗HIV病毒的药物,如奈非那韦、阿扎那韦、洛匹那韦和利托那韦等[25、26],能够与COVID-19组蛋白酶构象结合具有潜在的病毒抑制作用,由此可见许多抗病毒药物的使用均可能会导致新冠病毒检测的准确性。
总之目前病毒核酸检测出现假阴性问题是一个客观存在的现象,我们需要对其产生原因进行科学仔细的分析并且采取切实可行的措施不断提高病毒核酸检测的阳性率,降低假阴性率。充分发挥病毒核酸检测在新冠疫情防控中的作用。
五、关注核酸病毒检测的卫生投资效益问题
在当今乃至今后一个时期强调核酸检测的重大意义是毋庸置疑的,但是我们必须考虑到另一方面,即病毒核酸检测的投资效益问题。现在全员核酸检测一次少则几十万人,多则几百万,甚至上千万人。进入2022以后,许多地方核酸检测密度不断增加,开始是每个月一次,其后改为隔周一次,乃至每周一次,局地甚至每天一次。这样大面积、高密度检测核酸的代价是巨大的,包括人力和财力以及消耗大量的时间。进行任何一项卫生投资,哪怕是像目前这种紧急重大卫生投资也应该考虑到投资效益比,在疫情防控期间,尤其是现在这种外防输入内防反弹的特殊时期,大面积的检疫是必要的,然而如何提高病毒核酸检测阳性率则是需要认真考虑的一个大问题,建议国家卫生行政领导管理部门、CDC、科研机构和各大中医院认真关注这个问题,共同探讨如何尽快降低假阴性,提高诊断水平,而且应当将这个问题公之于众,使广大群众知情,更重要的是必须全面和准确的衡量和评估目前大面积、高频率核酸检测的真实效果和社会效益如何。
参考文献
[1]沈思鹏,魏永越,赵杨,等.全球新型冠状病毒肺炎疫情对我国的输入风险评估[J].中华流行病学杂志.2020,41(10):1582-1587.
[2]高翔,陈伟,郑丽,等.新型冠状病毒肺炎无症状感染者及其对疫情防控的挑战[J].中华流行病学杂志.2020,41(12):1985-1988.
[3]高文静,李立明.新型冠状病毒肺炎无症状感染相关研究进展[J].中华流行病学杂志.2020.41(4):485-488.
[4]Guan WJ, Ni ZY, Hu Y, et al. Clinical characteristics of coronavirus disease 2019 in China[J]. N Engl J Med, 2020, 382(18):1708-1720.DOI:10.1056/NEJMoa2002032.
[5]国家卫生健康委办公厅,国家中医药管理局办公室. 新型冠状病毒肺炎诊疗方案(试行第七版)[EB/OL]. (2020-03-04)[2020-04-20]. http://www.nhc.gov.cn/yzygj/s7653p/202003/46c9294a7dfe4cef80dc7f5912eb1989.shtml.
[6]汪明,吴青,徐万洲,等.8974例受检者新型冠状病毒核酸检测及合并感染结果分析[J].中华检验医学杂志,2020,43(4):31-35.
[7]里进,叶光明,陈良君,等.新型冠状病毒核酸检测假阴性结果原因分析及对策[J].中华检验医学杂志.2020,43(3):221-225.
[8]黎威,杜川,何青,等.咽拭子2019新型冠状病毒核酸阳性与阴性新型冠状病毒肺炎患者的临床特征比较.中华传染病杂志2020,38(10):655-658.
[9]李园园,雷宇,等.临床诊断新型冠状病毒肺炎中核酸检测阳性与阴性患者临床特征的比较[J].中华结核和呼吸杂志.2020,43(5):427-430.
[10]刘焱斌,刘涛,崔跃,等.鼻拭子与咽拭子两种取样方法在新型冠状病毒肺炎核算筛检中的比较研究[J].中国呼吸与危重监护杂志,2020,19(2):141-143.
[11]莫茜,秦炜,傅启华,等.正确认识新型冠状病毒核酸检测的影响因素[J].中华检验医学杂志,2020,43(3):213-216.
[12]王成彬.核酸检测用于确诊2019-nCoV核酸检测的影响因素[J].中华医学杂志,2020,100(13):961-964.
[13]张瑞,李金明.如何减少新型冠状病毒核酸检测的假阴性[J].中华医学杂志,2020,100(11):801-804.
[14]周灵,刘馗,刘辉国.新型冠状病毒肺炎患者出院后“复发”原因分析及治疗策略[J].中华结核和呼吸杂志,2020,43(4):281-284.
[15]智深深,许毅,陈耀凯,等.五例新型冠状病毒肺炎患者出院后核酸检测“复阳”的病例分析[J].中华检验医学杂志,2020,43(9):923-926
[16]王雪亮,徐幸,朱凯,等.新型冠状病毒核酸检测室间质量评价分析[J].中华检验医学杂志,2020,43(11):1100-1105.
[17]王成彬.核酸检测用于确诊新型冠状病毒肺炎阳性率低的原因分析[J].中华医学杂志,2020,100(13):961-964.
[18]Li XN, Shen XX, Li MH, et al. Applicability of duplex real time and lateral flow strip reverse-transcription recombinase aided amplification assays for the detection of Enterovirus 71 and Coxsackievirus A16[J]. Virol J, 2019,16(1):166.
[19]中国疾病预防控制中心新冠病毒肺炎应急响应机制流行病学组.新型冠状病毒肺炎流行病学特征分析[J].中华流行病学杂志,2020,41(2):145-151.
[20]中华人民共和国国家卫生健康委员会.新型冠状病毒感染的肺炎实验室检测技术指南(第三版)[EB/OL].2020-02-09.
[21]Corman VM, Landt O, Kaiser M, et al. Detection of 2019 novel coronavirus (2019-nCoV) by real-time RT-PCR[J]. Euro Surveill, 2020,25(3):2000045.
[22]Centers for disease control and prevention, respiratory viruses branch, division of viral disease. Real-time RT-PCR panel for detection 2019-novel coronavirus[EB/OL].(2020-02-04)[2020-02-14]. https://www.cdc.gov/coronavirus/2019-ncov/downloads/rt-pcr-panel-for-detection-instructions.pdf.
[23]World Health Organization. Coronavirus disease(COVID-19)technical guidance: laboratory testing for 2019-nCoV in humans[EB/OL].(2020-02-04)[2020-02-14].https://www.who.int/emergencies/disease/novel-coronavirus-2019/technical-guidance/laboratory-guidance.
[24]Phan T. Novel coronavirus: from discovery to clinical diagnostics[J]. Infect Genet Evol,2020,79:104211.
[25] Li Y, Zhang J, Wang N, et al.Therapeutic Drugs Targeting 2019-nCoV Main Protease by High-Throughput Screening[J]. BioRxiv,2020.922922
[26]Xu Z, Peng C, Shi Y, et al. Nelfinavir was predicted to be a potential inhibitor of 2019-nCov main protease by an integrative approach combining homology modelling, molecular docking and binding free energy caleulation[J]. BioRxiv, 2020.
(2021年6月7日第一稿,2022年10月28日第2稿)
发表评论
最新评论

-
new教师节特辑 | 北京医院刘明主任寄语:“敬畏生命、敬畏专业、敬畏未知”
2025-09-10 -
04-292025
人工智能诊疗将走向前台——医生做好准备了吗
-
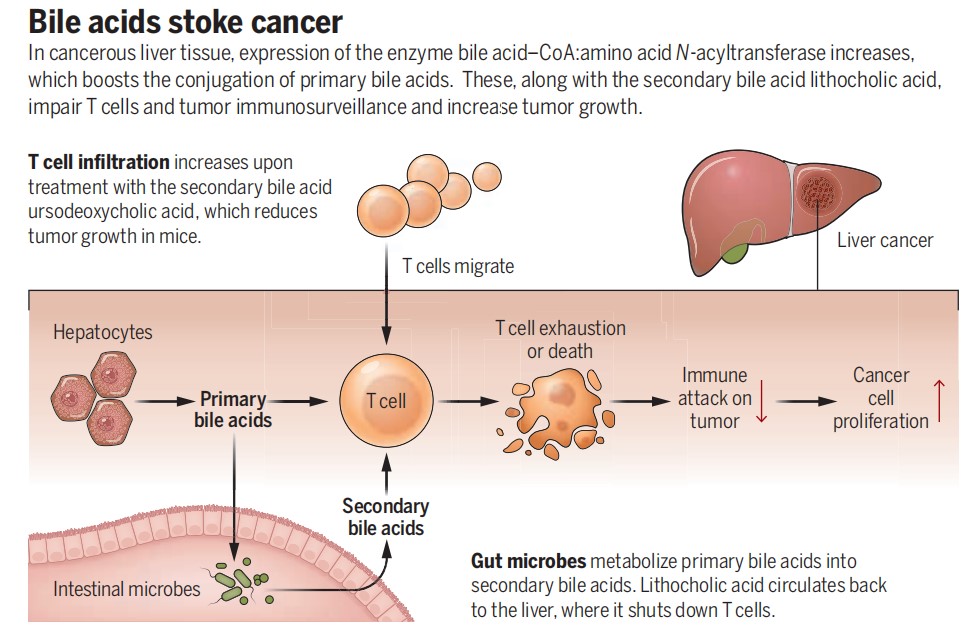
new肝癌免疫治疗的“路障”:胆汁酸 | 科普时光
2025-03-07 -
02-172025
慢病管理药先行 临床药师如何打通最后一公里
-

双镜合壁 助力消化疾病微创精准治疗
2024-12-24 -

朱玉龙:严重肺间质纤维化患者肺部结节经皮穿刺活检的注意事项
2024-11-21 -

IDSC感染专栏54③|重症感染患者弥散性血管内凝血早期诊断:中国诊断积分系统CDSS显优势
2022-06-28 -
IDSC感染专栏54②|夏秋季的烦恼,这种介于细菌与病毒间的病原在我国有抬头之势
2022-06-28 -
IDSC感染专栏54①|二代测序预测革兰阳性球菌耐药性有新发现
2022-06-28
-

何为巴林特小组?一文读懂
2017-02-23 -

IDSC感染专栏54③|重症感染患者弥散性血管内凝血早期诊断:中国诊断积分系统CDSS显优势
2022-06-28 -
益生菌预防艰难梭菌感染真的有效吗?
2021-09-07 -
孩子不是大人“缩微版” 小儿妇科聚焦未成年女性健康
2023-05-30 -

倪晓光:用好手中喉镜 提升鼻咽喉早癌检出率
2023-03-07 -
赵进喜教授:发挥中医药防治糖尿病肾脏病的特有优势
2023-06-09 -

心血管代谢医学|将临床研究融入社区日常临床诊疗以提高医学服务水平和质量
2021-11-05






