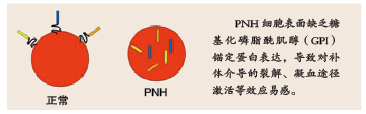
阵发性睡眠性血红蛋白尿症(PNH)是一种后天获得的溶血性疾病,主要临床表现包括骨髓衰竭、血管内溶血及血栓形成。近年来,抗补体C5单抗艾库组单抗的广泛使用,有效地控制了PNH的血管内溶血发作和血栓形成,同时治疗中出现一些新问题。
C5抑制剂疗效虽显著 但治疗新问题露头
有效控制血栓
西班牙的一篇报道称,16 例合并血栓的PNH患者应用艾库组单抗(Eculizumab)后,全部患者的血栓症状都得到缓解;只有1例患者在艾库组单抗治疗过程中出现血栓,此患者为房颤后短暂性脑缺血发作,使用抗凝药物治疗后仍然发作,在加大艾库组单抗剂量后好转。研究者得出结论:艾库组单抗对血栓并发症具有预防作用。此外,对PNH患者进行有创操作时,应监测乳酸脱氢酶水平并缩短艾库组单抗用药间隔。
对于PNH的血栓形成机制,目前仍有很多疑惑。荷兰学者Zeerleder等比较患者使用艾库组单抗前、后其中性粒细胞的活化和中性粒细胞细胞外网络(NET)形成情况。NET是一种强效促凝物质,中性粒细胞活化的血浆标志物如弹性蛋白酶-α1-抗胰蛋白酶复合物(EA)和核小体可作为NET的标志物。PNH患者的EA复合物与正常人类似,似乎不支持PNH患者中性粒细胞的活化。然而,在合并血栓的PNH患者中,核小体水平显著提高,提示低度NET的形成。在艾库组单抗治疗后,血栓组患者EA复合物的水平迅速、持续地下降,提示补体在中性粒细胞活化中发挥作用;核小体水平降低,提示艾库组单抗对PNH 的NET形成有抑制作用。
C3沉积引起血管外溶血
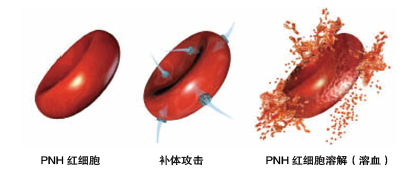
虽然艾库组单抗取得了良好疗效,但随着临床应用增多带来一些新问题。来自英国的报道称,C5抑制剂的使用保护了补体的早期成分,导致C3在PNH红细胞表面的堆积,或与CD55(C3衰变因子)缺失有关。大多数接受艾库组单抗的患者都有显著的血管外溶血,并出现临床症状。这种血管外溶血的出现,被认为与C3在PNH红细胞的堆积有关。
研究者对119例使用艾库组单抗的患者进行红细胞表面C3负荷检测。他们检测影响C3和FCγR的基因多态性,同时还检测46例使用艾库组单抗患者的具有功能的C3基因(rs2230199)的突变。结果发现,在119例使用艾库组单抗的患者中,110例PNH红细胞表面检测到C3,55例(46.2%)在治疗后还接受了至少1次输血(血管外溶血所致),其输血可能与C3的堆积有关。但是,同一患者的正常红细胞表面或未经艾库组单抗治疗患者的红细胞上,并未出现C3的沉积。
研究者分析Fcγ受体的一种有功能性的多态性表现,但并未发现与血液学参数相关。而具有C3S纯合子多态性的患者在艾库组单抗治疗后,红细胞出现显著的C3的沉积,网织红细胞和胆红素水平也明显增高。该研究首次证明,C3基因具有功能性的多态性基因与艾库组单抗使用后血管外溶血的参数增加有关,而C3 抑制剂APL-1和APL-2可保护PNH红细胞的C3沉积,从而显著减少血管外溶血。
C5突变致疗效欠佳
随着艾库组单抗在亚洲的广泛使用,日本学者报道了11例患者由于少见的基因多态性导致对C5单抗反应不佳。早在2012年,日本学者就报道了29例使用 艾库组单抗的PNH患者,有2例反应不佳。至今,共报道300例患者使用艾库组单抗,11例反应不佳。
为明确不同患者对艾库组单抗反应的差异性,研究者检测了反应良好和不佳患者的外周血样本。反应不佳者血液中艾库组单抗浓度已超过达到疗效所需的浓度,患者依然反应不佳。然而,体外使用另外一种C5单抗时,这些患者红细胞的溶血活性在却被阻止。
通过DNA测序,在反应不佳患者中检测到C5外显子21单个杂合性错意突变:c.2654G>A的突变,肽链为p.Arg885His,而在反应良好患者中未检出。这些突变在正常人的检出率与反应不佳者相同。关于这种多态性,在120例正常中国人对照者中有1例被检出,而在100例英国裔及90例墨西哥裔人中并未检出。在体外实验中,虽然有突变的rC5m和没有突变的rC5的功能类似,但rC5m却不能被艾库组单抗所阻断。结果提示,C5突变导致艾库组单抗对其阻断不佳是患者对药物反应不好的原因。
C3抑制剂或开启治疗新途径
虽然C5抑制剂艾库组单抗疗效良好,但价格昂贵;虽然有效抑制了红细胞的血管内溶血,但并不能阻止补体成分C3片段的活化及最终导致免疫细胞引起血管外溶血。因此,人们正在探索使用C3抑制剂控制PNH红细胞血管外溶血的可能。
Compstatin是一种选择性结合人类C3主要成分的多肽,可以防止C3向C3b转化,从而抑制补体活化的最终途径。由于Compstatin对C3活化可能的抑制以及多肽类药物相对低的制造成本,Compstatin类似物(早期主要用于治疗黄斑部退化)对PNH的治疗是一个很有前景的药物。
2013年美国血液学会年会上,美国学者Ricklin等报道在实验动物猴子使用第二代Compstatin类似物并探索合适剂量的研究。在体外实验中,第二代Compstatin类似物及其脂质体衍生物可很好地防止补体活化,防止补体介导的溶血。研究者还对这些药物进行了药代动力学研究,并在动物身上得到了很好验证。结果提示,Compstatin类似物可抑制所有补体介导溶血的作用,其可能的临床应用将为PNH的治疗打开新途径。