2016年NCCN成人癌痛指南解读
首次明确癌痛管理“4A”目标,强调阿片类药物是癌痛治疗的基石
癌症相关性疼痛是指肿瘤直接引起的疼痛,或是特殊治疗带来的疼痛。癌症相关疼痛严重影响癌症患者的生活质量,甚至造成患者治疗中断。
目前,癌痛治疗已成为肿瘤治疗尤其是肿瘤姑息治疗的重要组成部分,也是肿瘤专科医生关注的热点之一。
一直以来,美国国家综合癌症网络 (NCCN)成人癌痛指南得到了广大临床医师的认同和推行。
2月22日,NCCN发布了2016 年成人癌痛临床实践指南第一版(简称“新指南”)。新指南仅对其中部分条目进行了修订,但一些内容的加入更加凸显了癌痛治疗过程的人性化。
因此,本期邀请了北京肿瘤医院姑息治疗中心刘巍教授及陕西省肿瘤医院中西医结合科吴敏慧教授等就新指南的更新要点进行解读,以便指导医生临床实践。

新指南整体仍强调5项主要内容,包括癌痛的评估与再评估、癌痛药物的应用、辅助药物的应用、阿片类药物不良反应的处理、患者教育及社会支持。
新指南最大亮点是明确了癌症管理的目标及如何处理阿片类药物的不恰当应用等。
新指南更新要点
疼痛管理应达到“4A”目标
优化的镇痛(Optimize Analgesia)
优化的日常生活(Optimize Activities of daily living)
最小的不良反应(Minimize Adverse effects)
避免不恰当给药(Avoid Aberrant drug taking)
新指南在癌痛管理原则中指出,癌痛的最佳治疗是多学科团队综合治疗,口服缓释制剂依然是治疗癌痛最常见的首选给药途径;并首次明确强调疼痛管理应达到“4A”目标,即优化的镇痛、优化的日常生活、最小的不良反应、避免不恰当给药。目的是既要追求患者的舒适度、改善功能,又要保证安全。四项目标也正是整个指南的精要之处,需要临床医师和患者及家属践行。
以最大限度改善患者为首要标准
在临床实践部分里的阿片类使用原则、处方、滴定和维持内容方面,特别强调了以最大限度改善患者为首要标准;增加了“长期阿片类药物治疗过程中,要保证患者安全用药,最大限度减少阿片类药物滥用者风险的策略”的指导,建议加强阿片类药物不恰当应用的风险评估,更加关注患者及家属教育,建议加强社会支持服务,其中一些方法可供国内临床医生参考。
1,加强阿片类药物不恰当应用的风险评估,使用预测性好、可靠度高的评估工具。指南中推荐在服用阿片类药物前应用癌痛患者筛查及阿片类药物应用评估(SOAPP-R)及阿片类药物风险评估工具(ORT)进行评估,在应用药物过程中可以应用阿片类药物误用情况评估表(COMM)实时监测评估。
2,为确保药物反应不会干扰患者的正常治疗,需加强患者教育,主要让患者及家属认识到阿片类药物治疗的获益及潜在风险,特别是要充分了解药物的不良反应及阿片类药物潜在的误用、滥用、成瘾风险。
3,加强高危患者的支持服务:主要针对前期评估中存在一项或多项阿片类药物误用、滥用风险的患者。特别是行为干预及行为认知干预有助于患者提高处理问题的能力,降低自身风险因素,而从中获益。
4,在高危情况下,可采取一些简单易行的方法增强医师和患者对自身的观察监测:
★建议患者建立一个用以记录药物的使用剂量及时间的“镇痛药物使用日记”;
★医师使用药片计数的方法,来核实门诊患者“镇痛药物使用日记”中记录的信息;
★在治疗基线时和治疗期间行尿检,可以监测不恰当的药物使用,从而提高患者的依从性;
★对于出现药物不恰当使用或存在高危因素的患者,可适当增加门诊就诊频率,视情况适当减少每次处方的药物剂量。
5,教育患者及家属对限制药品的处置、储藏、处理,以保持社区的安全,使社区中阿片类药物误用、滥用情况降到最低。如在有能力处理多余限制药品的社区中,鼓励开展“回收项目”;此外,FDA在“安全用药指导”的“处理未使用药物:你应该知道”一文中建议可以将多余的阿片类药物冲进厕所。同时,还应教育患者及家属不要与家人和朋友分享阿片类药物等。
注重阿片类药物不良反应
在阿片类药物不良反应管理部分,也进行了细微调整,对便秘的防治进行了增补和修正。
在“便秘-如果便秘持续存在”一节中增加了“重新评估便秘的原因和严重程度,排除肠梗阻修正为排除肠梗阻和高钙血症,并评估其他有可能与便秘相关的药物的影响”;细化了药物用量,包括番泻叶的最大剂量由每天8~12片修正为每天8片;聚乙二醇的使用剂量修正为口服2次/d,每次1满汤匙=17 g(8盎司);同时增加了新的二线治疗药物,包括鲁比前列酮和纳洛西酮(FDA批准用于阿片类药物诱发性便秘),以及利那洛肽(FDA批准用于特发性便秘)。
此外,新指南还修订了部分便秘及谵妄的不良反应的处理。

发表评论
最新评论

-
04-292025
人工智能诊疗将走向前台——医生做好准备了吗
-
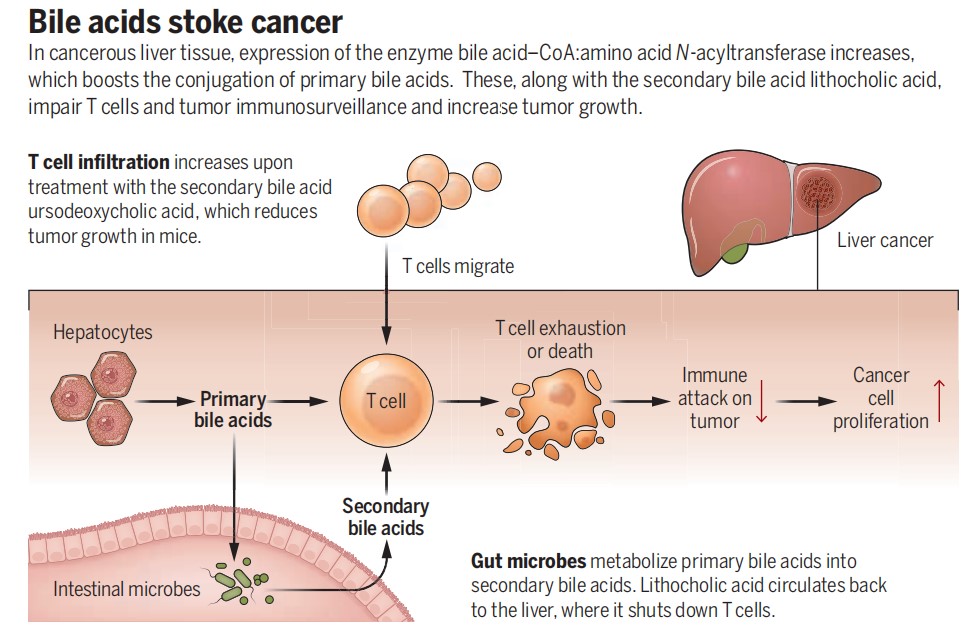
new肝癌免疫治疗的“路障”:胆汁酸 | 科普时光
2025-03-07 -
02-172025
慢病管理药先行 临床药师如何打通最后一公里
-

new双镜合壁 助力消化疾病微创精准治疗
在精准治疗、功能保护越来越多地被重视的情况下,内镜与腹腔镜“双镜联合”成为胃肠疾病诊疗的一种趋势。
2024-12-24
-

双镜合壁 助力消化疾病微创精准治疗
2024-12-24 -

朱玉龙:严重肺间质纤维化患者肺部结节经皮穿刺活检的注意事项
2024-11-21 -

IDSC感染专栏54③|重症感染患者弥散性血管内凝血早期诊断:中国诊断积分系统CDSS显优势
2022-06-28 -
IDSC感染专栏54②|夏秋季的烦恼,这种介于细菌与病毒间的病原在我国有抬头之势
2022-06-28 -
IDSC感染专栏54①|二代测序预测革兰阳性球菌耐药性有新发现
2022-06-28
-

何为巴林特小组?一文读懂
2017-02-23 -

IDSC感染专栏54③|重症感染患者弥散性血管内凝血早期诊断:中国诊断积分系统CDSS显优势
2022-06-28 -
益生菌预防艰难梭菌感染真的有效吗?
2021-09-07 -
孩子不是大人“缩微版” 小儿妇科聚焦未成年女性健康
2023-05-30 -
赵进喜教授:发挥中医药防治糖尿病肾脏病的特有优势
2023-06-09 -

倪晓光:用好手中喉镜 提升鼻咽喉早癌检出率
2023-03-07 -

心血管代谢医学|将临床研究融入社区日常临床诊疗以提高医学服务水平和质量
2021-11-05






