美国梅奥中心近日发文,质疑FDA近几年批准的抗癌药物,1/3以上(19/83,37%)疗效依靠替代终点来证实,且未分析是否真正转化为患者的生存获益,即这些药物可能是无用的。更糟糕的是,由于这些药物已被批准,即使后续试验证实没有生存获益,作为加速审批的一项条件,这些药物也不会被废除批准。(Mayo Clinic Proceedings.5月20日在线版 )
对抗癌药物,FDA目前有两种审批机制,一种是传统审批流程(TA),一种是加速审批(AA)。近年来,几乎所有加快审批过程都采取了用“替代终点”(即不等到真正的终点事件发生,而选取某个事件来代替终点)来审核药物效果的方案,而传统审批流程也越来越多地采用这种方式。
梅奥中心分析了2009-2014年FDA批准的83个抗肿瘤药物,其中55个以“替代终点”获批(25个为加速审批,30个为传统审批流程)。
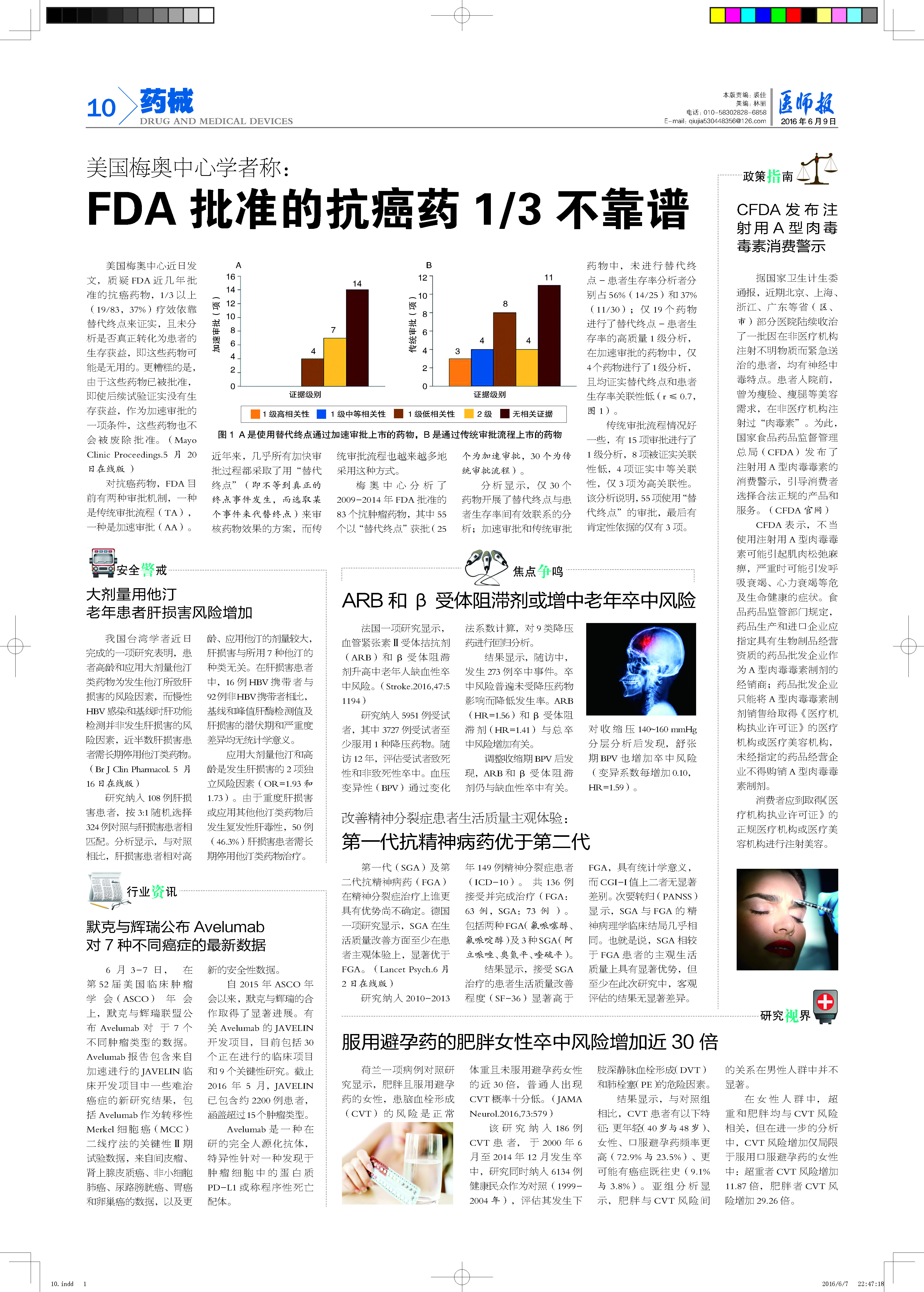
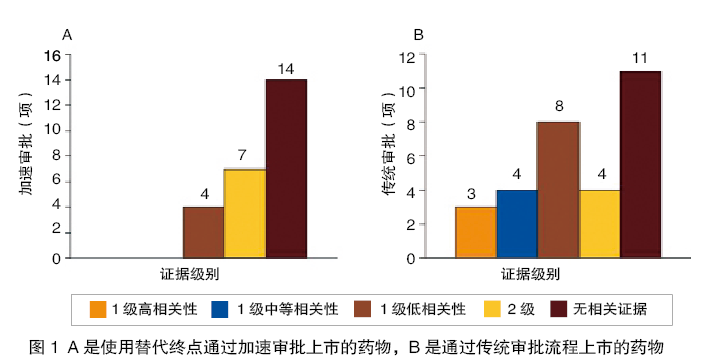
分析显示,仅30个药物开展了替代终点与患者生存率间有效联系的分析;加速审批和传统审批药物中,未进行替代终点-患者生存率分析者分别占56%(14/25)和37%(11/30);仅19个药物进行了替代终点-患者生存率的高质量1级分析,在加速审批的药物中,仅4个药物进行了1级分析,且均证实替代终点和患者生存率关联性低(r≤0.7,图1)。
传统审批流程情况好一些,有15项审批进行了1级分析,8项被证实关联性低,4项证实中等关联性,仅3项为高关联性。该分析说明,55项使用“替代终点”的审批,最后有肯定性依据的仅有3项。