抗病毒是治疗慢性乙肝的关键
据世界卫生组织报道,全球约20亿人感染HBV,其中6.9亿人在中国;全球乙型肝炎病毒表面抗原(HBsAg)携带者3.5亿,其中1/3在中国;全世界每年75万人死于HBV感染引起的疾病,其中28万来自中国,并且其中25%~40%最终将死于肝硬化和肝癌。为了规范乙型肝炎的治疗及预防,中华医学会肝病学分会、感染病学分会于2010年出台了《慢性乙肝防治指南》,作为指南制定的主要参与者,上海交通大学附属第一人民医院消化科陆伦根教授对此进行了解读。
抗病毒可延缓肝硬化加重
慢性乙肝之所以进展为肝硬化,罪魁祸首当属乙型肝炎病毒(HBV),Iloeje UH等对3582例受试者13年随访中发现,随着基线HBV DNA的升高,肝硬化发生率也增加。这是由于HBV未能较好抑制,肝细胞炎症也就不能被很好控制,进而形成肝纤维化,最终发展成肝硬化。即从肝炎-肝纤维化-肝硬化,病毒始终在起作用,所以乙肝肝硬化的治疗重点是抗病毒。
乙肝患者发展到到肝硬化阶段,并非必定走向肝衰竭而死亡,如果能抑制病毒,去除或减轻病毒作用,可阻止或延缓肝硬化加重甚至发展为肝癌,同时患者也可获得较好的生活质量。Liaw YF等研究表明,早期肝硬化患者抗病毒治疗可减少疾病进展为失代偿、肝癌、自发性细菌性腹膜炎、出血性食管静脉曲张以及肝病引起的死亡。另外抗病毒治疗还可显著减少患者的并发症,且提高失代偿患者的生存率。
《慢性乙肝防治指南》关于肝硬化抗病毒治疗指征规定:在代偿期肝硬化患者中,若乙型肝炎e抗原(HBeAg)阳性,HBV DNA≥104 cp/ml或HBeAg阴性,HBV DNA≥103 cp/ml时,无论谷丙转氨酶(ALT)正常或升高均应行抗病毒治疗。而在失代偿肝硬化患者中,只要能检出HBV DNA,则无论ALT是否升高,都应在知情同意基础上,及时应用核苷酸类药物抗病毒治疗。
抗病毒药物应首选核苷酸类似物
当前抗病毒药物主要包括干扰素类以及核苷酸类药物。其中核苷酸类药物包括拉米夫定(LAM)、阿德福韦酯(ADV)、恩替卡韦(ETV)、替比夫定(LDT)以及替诺福韦酯(TDF)等。干扰素会加重肝脏疾病且价格昂贵,因此国内使用较少,而核苷酸类药物治疗安全性和耐受性良好。因此指南规定,代偿期肝硬化患者使用干扰素时要慎重,而对失代偿肝硬化患者则应完全禁用干扰素。指南还推荐,两类患者均应选用核苷酸类药物治疗。
核苷酸类药物虽然总体安全性、耐受性良好,但是不同药物还会影响身体的不同机能,再加之抗病毒治疗的长期性以及肝脏代谢功能障碍导致的药物及其代谢产物在体内的蓄积。因此使用时需加强安全性监测,包括生物化学、病毒学、血常规、血清肌酐和肌酐激酶等指标的监测。
核苷酸类药物最大的障碍是耐药
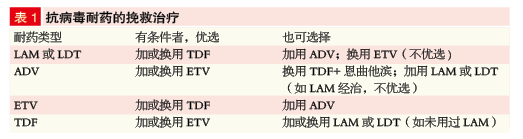
应用核苷酸类药物最大的障碍是耐药。因此在治疗时要严格掌握治疗适应证,谨慎选择核苷酸类药物,初始选用强效和高耐药性基因屏障药物如ETV、TDF的单药长期治疗,尽量避免低耐药性基因屏障药物的单药序贯治疗。治疗过程中,密切监测HBV DNA,一旦出现耐药信号,尽快进行耐药基因位点的检测,对已确认的耐药,应及早进行挽救治疗,避免可能出现的肝脏功能失代偿、急性肝衰竭甚至死亡的风险。出现耐药后,最好的办法就是改用其他治疗方案(表1)。
供体缺乏是阻碍肝脏移植发展的最大瓶颈
全国首例减体积儿童肝脏移植者于2000年在天津市第一中心医院由朱志军、沈中阳等成功实施。13年后,李扬回院庆“重生”。
首都医科大学附属北京友谊医院朱志军教授指出,我国肝移植始于20世纪70年代,期间由于供体缺乏、费用昂贵、预后不佳等原因一度处于停滞状态,直到进入21世纪,肝脏移植的数量才逐年倍增,至今已有两万多患者受益于肝移植,肝移植受者中,成人病因以乙型肝炎为主,儿童病因以wilon’s和先天性肝病为主。目前受者第一年、三年、五年的总体累计生存率已达到77.97%、65.38%、60.53%。
把控肝脏移植最佳时机
肝脏移植是治疗终末期肝脏疾病的唯一有效方法。当有肝移植适应证(图1)的患者出现反复的食管-胃底静脉曲张破裂出血、顽固性腹水、肝肾综合症、自发性细菌性腹膜炎、严重凝血功能障碍、重度黄疸所致严重瘙痒或肝性脑病时,意味着肝功能严重不全,生存时间极短,应尽快采取肝脏移植手术。研究表明,终末期肝病模型评分(MELD Score)<15的患者在接受肝移植1年后生存率与相同状态继续等待的患者近似,甚至死亡率会高于仍在等待的患者。肝移植患者术前等待供肝需要很长时间,因此上述患者应在MELD Score>15,病情尚平稳时尽早作出决策,早日进入等待肝移植的行列。这在移植效果和治疗费用上也更为有利。

面对供体瓶颈应提高器官利用率
随着肝脏移植技术日渐成熟,供体缺乏、受体增多的矛盾在我国日益突出,已成为抑制我国肝移植手术的一个最大瓶颈。欧美国家脑死亡供体是最主要的肝脏供体来源,但我国对脑死亡的认识与接收程度还较低,因此在国家层面上应呼吁民众加强器官捐献的意识外。此外外科医生还应通过自身技术手段提高器官利用率。
劈离式肝脏移植是将完整的供肝按照正常解剖结构,修整分离出两套各自独立的动脉、门静脉、肝静脉及胆道系统,分别提供给两位受者完成肝移植。该项手术的关键技术是劈离供肝。国外通常是在供者脑死亡但心脏仍在跳动的情况下,在供者体内将一个供肝劈成两半。限于国情,我国施行此类手术,只能在体外完成肝劈手术,增加了并发症的风险。劈离式肝脏移植只适用于一个成人和小孩之间的移植。而朱教授完成的亚洲首例肝中静脉完全劈分劈离式肝移植可使用于两个成人间的肝移植。此外解决器官匮乏的途径还有边缘供体、以及交叉辅助式肝移植的使用。







