
EORTC 18071研究:
伊匹单抗辅助治疗黑色素瘤获明显生存获益
来自法国Alexander Eggermont教授公布了研究结果,纳入951例3期黑色素瘤患者,行完成切除术,之后随机分入试验组(伊匹单抗 10mg/kg,q3w,4周期,随后每3月1次直至术后满3年)或安慰剂组。主要研究终点为达到无复发生存期(RFS),随访5.3个月。
结果显示,RFS获益转换为生存获益,试验组死亡风险下降28%(总生存期HR 0.72,95%CI 0.58~0.88,P=0.001),远处转移风险下降24%(HR 0.76,95%CI 0.64~0.92,P =0.002)。5年生存率(OS)试验组为65%,安慰剂组为54%,提高11%。试验组3~4级胃肠道反应为16%,肝脏不良反应为11%,内分泌不良反应为8%。
研究解析——
另一项研究比较伊匹单抗不同剂量对于未接受过BRAF或免疫检查点抑制剂治疗的3~4级黑色素瘤患者的疗效。研究分为高剂量组伊匹单抗(10 mg/kg,q3w,4周期)与低剂量组(3 mg/kg)。结果显示,高、低剂量组中位OS为15.7个月和11.5个月。在高剂量组中不良反应更重,但效果更佳。由此可见,伊匹单抗疗效与剂量相关。
ENGOT-OV16/NOVA 研究:
Niraparib显著提高铂类敏感的复发性卵巢癌的无进展生存
丹麦哥本哈根大学医院Mansoor Raza Mirza教授公布了该Ⅲ期研究结果,研究纳入553例对铂类敏感的复发性卵巢癌患者,其中203例为BRCA突变,350例无突变。按照BRCA突变状态分层,分为试验组和安慰剂组。
结果显示,Niraparib在突变或无突变的患者中均取得效果。在BRCA突变者中,试验组与安慰剂组中位PFS为21.0个和5.5个月。BRCA无突变者中,两组中位PFS为9.3个月和3.9个月。在BRCA无突变,担忧同源重组DNA修复缺陷(HRD)中,两组中位PFS为12.9个月和3.8个月。
Niraparib组有超过10%的患者有3~4级不良反应。剂量调整后治疗可继续。试验组症状控制更好,生存质量更高。
研究解析——
Niraparib提高了总体和各层中第二次PFS时间,接受后续第1次治疗时间间隔,无化疗时间间隔等。鉴于铂类敏感的复发性卵巢癌占所有卵巢癌患者的70%,而该研究中Niraparib延长PFS的效果与BRCA基因突变状态无关,明显延长的PFS表明PAPR抑制剂在卵巢癌患者治疗中的重要作用。
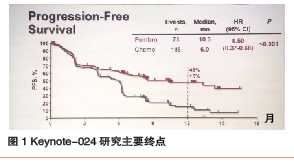
Keynote-024研究:
帕姆单抗或为晚期非小细胞肺癌一线治疗
德国Martin Reck教授公布了这一Ⅲ期临床试验结果,帕姆单抗(Pembrolizumab)显然已成为PD-L1高表达进展期肺癌的一线治疗新选择。
高PD-L1表达的晚期NSCLC占总体晚期NSCLC的27%~30%。研究比较了初诊高PD-L1表达(≥50%的肿瘤细胞表达)的晚期NSCLC患者帕姆单抗对比标准含铂方案化疗疗效。EGFR突变或ALK转座被排除在外。
该研究纳入305例患者,随机分入帕姆单抗组和化疗组。44%的化疗组患者疾病进展后可进入帕姆单抗组作为二线治疗。试验组和化疗组PFS分别为10.3个月与6.0个月(HR 0.50,图1),帕姆单抗提高了4个月。OS也有所提高,帕姆单抗组6月生存率为80%,化疗组为72% (HR 0.60)。由于44%的化疗组患者以帕姆单抗为二线治疗,因此帕姆单抗所带来的总生存获益实际上更显著。
研究表明,帕姆单抗组总缓解率高于化疗组(45%与28%),缓解时间更长,所有3/4级不良反应发生率更低。
研究解析——
《新英格兰医学杂志》在评论中指出,这项研究将完全改变进展期NSCLC患者的治疗模式,所有研究结果都在指示,Pembrolizumab将会成为PD-L1阳性、未经治疗的晚期NSCLC患者的新的治疗标准。
而中国临床肿瘤学会理事长吴一龙教授也感叹:“变天了! 10月9日下午5时,哥本哈根会议中心见证了这一历史性的时刻:针对哨卡点的免疫治疗,赢了近100年晚期肺癌治疗的基石——化学治疗。无论从有效率、无进展生存还是总生存,赢得利落、赢得干脆、赢得对手没话说。”
Monaleesa 2研究:
Ribociclib联合来曲唑一线治疗HR+HER2-乳腺癌获明显临床获益
主要研究者Gabriel Hortobagyi教授介绍,目前CDK4/6抑制剂已上市药物有Palbociclib、Abemaciclib、Ribociclib(LEE011)。前两种药物已经获批,Monaleesa 2研究的公布,使得Ribociclib联合来曲唑一线治疗HR+HER2-晚期或转移性乳腺癌也被FDA授予突破性药物资格。
该研究纳入668例HR+HER2-乳腺癌患者。患者既往未接受任何系统性治疗,随机分为Ribociclib+来曲唑联合治疗(Ribociclib 600mg/d,3w休息1周,来曲唑 2.5 mg/d,持续用药)或安慰剂+来曲唑组治疗。主要终点是PFS,次要终点包括OS、ORR、临床获益率(CBR)等。
结果显示,安慰剂+来曲唑组患者中位PFS为14.7个月,Ribociclib+来曲唑治疗组中位PFS未达到,但95%CI不小于19.3个月,说明PFS至少提高44%(HR 0.556,P= 0.00000329)。Ribociclib+来曲唑治疗组客观反应率更高(53%与37%,P=0.00028),临床获益率更高(80% 与72% P=0.02)。
研究表明,两组严重不良反应发生率均低于5%。但Ribociclib+来曲唑治疗组的常见不良反应发生率更高。OS终点均未达到。
研究解析——
该研究是继PALOMA2后CDK4/6抑制剂在HR+HER-晚期绝经后乳腺癌治疗领域的又一突破,颠覆了过去数十年间HR+HER-晚期绝经后乳腺癌单一内分泌治疗的陈旧模式。CDK4/6抑制剂联合其他信号通路抑制剂或成为乳腺癌特定亚型治疗的研究热点。
Checkmate 141研究:
Nivolumab可缓解复发转移性头颈部肿瘤的症状并维持其功能
研究纳入361例铂类耐药的复发头颈部肿瘤患者。分为Nivolumab组和标准化疗组(按医生要求使用MTX,多西他赛或西妥昔单抗)。Nivolumab能提高2.5个月的总生存时间。129例患者完成基线,用药9周和间隔6周后的调查问卷。结果显示,Nivolumab组功能和症状在9周和15周时得到维持甚至改善,化疗组较差。比较9周和15周的评分时,Nivolumab组在绝大多数功能和症状评分显著优于化疗组。
研究解析——
Nivolumab不仅能带来生存获益,且能维持头颈部肿瘤患者的功能,改善其症状。这可能与其药物不良反应减少有关。免疫治疗向传统的“No pain,No gain”的治疗模式提出了挑战。头颈部肿瘤患者通常有很多症状的困扰,如颈部肿块引起的疼痛、进食受限和言语受限。选择不良反应更少的药物有其独特的优势。Nivolumab仅对1/3的晚期头颈部肿瘤患者有益,需有生物标记物帮助辨明这些患者以减少不良反应及不必要的医疗费用。







